Виды растворов. Виды концентрации растворов
Растворы – это состоящая из двух или более веществ однородная масса или смесь, в которой одно вещество выступает в качестве растворителя, а другое – в качестве растворяемых частиц.
Существует две теории трактовки происхождения растворов: химическая, основоположником которой является Менделеев Д. И., и физическая, предложенная немецким и швейцарским физиками Оствальдом и Аррениусом. Согласно трактовке Менделеева, компоненты растворителя и растворяемого веществ становятся участниками химической реакции с образованием неустойчивых соединений этих самых компонентов или частиц.
Физическая же теория отрицает химическое взаимодействие между молекулами растворяющего и растворяемого веществ, объясняя процесс образования растворов как равномерное распределение частиц (молекул, ионов) растворителя между частицами растворяемой субстанции вследствие физического явления, именуемого диффузией.
Классификация растворов по различным критериям
На сегодня нет единой системы классификации растворов, однако условно виды растворов можно сгруппировать по наиболее значимым критериям, а именно:
I) По агрегатному состоянию выделяют: твёрдые, газообразные и жидкие растворы.
II) По размерам частиц растворённого вещества: коллоидные и истинные.
III) По степени концентрации частиц растворённого вещества в растворе: насыщенные, ненасыщенные, концентрированные, разбавленные.
IV) По способности проводить электрический ток: электролиты и неэлектролиты.
V) По назначению и области применения: химические, медицинские, строительные, специальные растворы и др.
Виды растворов по агрегатному состоянию
Классификация растворов по агрегатному состоянию растворителя приводится в широком смысле значения этого термина. Принято считать растворами жидкие субстанции (причём в качестве растворяемого вещества может выступать как жидкий, так и твёрдый элемент), однако если учесть тот факт, что раствор – это гомогенная система из двух или нескольких веществ, то вполне логично признать также и твёрдые растворы, и газообразные. Твёрдыми растворами принято считать смеси, например, нескольких металлов, больше известных в обиходе как сплавы. Газообразные виды растворов – это смеси нескольких газов, пример – окружающий нас воздух, который представлен в виде соединения кислорода, азота и углекислого газа.

Растворы по размеру растворённых частиц
Виды растворов по размеру растворённых частиц включают истинные (обычные) растворы и коллоидные системы. В истинных растворах растворяемое вещество распадается на мелкие молекулы или атомы, по размерам приближённые к молекулам растворителя. При этом истинные виды растворов сохраняют первоначальные свойства растворителя, лишь слегка преображая его под действием физико-химических свойств добавленного в него элемента. Например: при растворении поваренной соли или сахара в воде вода остаётся в том же агрегатном состоянии и той же консистенции, практически такого же цвета, меняется только её вкус.

Коллоидные растворы отличаются от обычных тем, что добавляемый компонент распадается не полностью, сохраняя сложные молекулы и соединения, размеры которых значительно превышают частицы растворителя, превосходя значение 1 нанометра.
Виды концентрации растворов
В одно и то же количество растворителя можно добавить разное количество растворяемого элемента, на выходе будем иметь растворы с разной концентрацией. Перечислим основные из них:
- Насыщенные растворы характеризуются степенью растворимости вещества, при которой растворяемый компонент под влиянием постоянной величины температуры и давления больше не распадается на атомы и молекулы и раствор достигает фазового равновесия. Насыщенные растворы также условно можно разделить на концентрированные, в которых массовая доля растворённого компонента сопоставима с растворителем, и на разбавленные, где растворённого вещества в несколько раз меньше растворителя.
- Ненасыщенные – это те растворы, в которых растворяемое вещество ещё может распадаться на мелкие частицы.
- Пересыщенные растворы получаются тогда, когда изменяются параметры воздействующих факторов (температура, давление), в результате чего продолжается процесс «дробления» растворённого вещества, его становится больше, чем было при нормальных (обычных) условиях.
Электролиты и неэлектролиты
Некоторые вещества в растворах распадаются на ионы, способные проводить электрический ток. Такие гомогенные системы называются электролитами. В эту группу входят кислоты, большинство солей. А растворы, не проводящие электрический ток, принято называть неэлектролитами (почти все органические соединения).

Группы растворов по назначению
Растворы незаменимы во всех отраслях народного хозяйства, специфика которых создала такие виды специальных растворов, как медицинские, строительные, химические и другие.
Медицинские растворы – это совокупность препаратов в форме мазей, суспензий, микстур, растворов для инфузий и инъекций и прочих лекарственных форм, применяемых в медицинских целях для лечения и профилактики различных заболеваний.
Виды химических растворов включают в себя огромное множество гомогенных соединений, используемых в химических реакциях: кислоты, соли. Эти растворы могут быть органического или неорганического происхождения, водные (морская вода) или безводные (на основе бензола, ацетона и т. д.), жидкие (водка) или твёрдые (латунь). Они нашли своё применение в самых различных отраслях национального хозяйства: химическая, пищевая, текстильная промышленность.
Виды строительных растворов отличаются вязкой и густой консистенцией, из-за чего им больше подходит название смеси.
 Благодаря своей способности быстро затвердевать они с успехом применяются в качестве вяжущего материала для кладки стен, потолков, несущих конструкций, а также для отделочных работ. Представляют собой водные растворы, чаще всего трёхкомпонентные (растворитель, цемент различных маркировок, заполнитель), где в качестве наполнителя используется песок, глина, щебень, известь, гипс и другие строительные материалы.
Благодаря своей способности быстро затвердевать они с успехом применяются в качестве вяжущего материала для кладки стен, потолков, несущих конструкций, а также для отделочных работ. Представляют собой водные растворы, чаще всего трёхкомпонентные (растворитель, цемент различных маркировок, заполнитель), где в качестве наполнителя используется песок, глина, щебень, известь, гипс и другие строительные материалы.fb.ru
Виды растворов
2
РАСТВОРЫ
Растворы однородные смеси двух или большого числа веществ (компонентов), которые равномерно распределены в виде отдельных атомов, ионов, молекул.
Различают истинные, коллоидные растворы и суспензии.
Истинные растворы характеризуются прозрачностью, имеют малые размеры растворённых частиц, легко проходят через биологические мембраны. В зависимости от концентрации солей существует три типа растворов: изотонические; гипертонические; гипотонические;
1. И з о т о н и ч е с к и е р а с т в о р ы имеют одинаковую концентрацию солей, как и в плазме крови, и такое же осмотическое давление.
К ним относят растворы, имеющие концентрацию солей 0,9%.
Одним из таких растворов является физиологический раствор —
С кл = С раствор С – концентрация солей
Н2 0
В этом растворе клетка сохраняет все жизненно важные функции, осуществляя процессы дыхания, размножения, обмена веществ.
Применение физиологического раствора.
Вводят физраствор через рот, внутривенно, внутримышечно, подкожно, в прямую кишку:
при некоторых заболеваниях – тяжелые длительные поносы, холера, неукротимая рвота, обширные ожоги хлорид натрия выделяется из организма в больших количествах, чем обычно. Также его много теряется с потом при работе в горячих цехах. В таких случаях в организме возникает его недостаточность, что сопровождается развитием ряда болезненных явлений: спазмы, судороги, нарушения кровообращения, угнетение ЦНС;
при интоксикациях, кровопотерях, обезвоживании, высокой температуре
для промывания глаз, носовой полости.
натрий хлористый является составной частью растворов применяющихся в качестве кровозамещающих (плазмозамещающих) жидкостей.
2. Г и п е р т о н и ч е с к и й р а с т в о р (2%, 5%, 10%, 15%) —
К ним относятся растворы, содержащие более 0,9% солей. Если клетку поместить в такой раствор, то вода из клетки поступает в окружающую среду, при этом падает в клетке тургорное (осмотическое) давление, содержимое клетки сжимается, она теряет форму, происходит обезвоживание. Это явление называется — плазмолиз
. С кл < С раствор
Н2 0
Явление
плазмолиза обратимое, если поместить
клетку в гипотонический раствор, то в
таком растворе она восстановит объем
и форму Н
Применяют гипертонический раствор для:
полосканий горла, для ванн, обтираний;
назначают при запорах для опорожнения кишечника.
в виде компрессов и примочек применяются при лечении гнойных ран, раны очищаются от гноя;
2 – 5% растворы используют для промывания желудка при отравлении нитратом серебра;
внутривенно используют при отёке лёгких и внутренних кровотечениях.
3. Г и п о т о н и ч е с к и й р а с т в о р, это раствор, имеющий меньшую концентрацию солей, чем в плазме крови.
С кл > С раствор
Н2 0
Животные
клетки, в таком растворе быстро разрушаются
т.к. мембрана не выдерживает высокого
осмотического давления и разрывается.
Это явление называется цитолиз.
Частные случаи цитолиза – разрушение
эритроцитов крови – гемолиз, при этом гемоглобин выходит в плазму
крови и окрашивает ее в красный цвет,
такая кровь называется
Растительные клетки в таком растворе обычно только набухают, т.к. имеют кроме цитоплазматической мембраны плотную клеточную стенку – целлюлозную оболочку. Но, если растительные клетки длительно находятся в гипотоническом растворе, то и они разрушаются.
Применяют гипотонические растворы в качестве растворителей для водорастворимых лекарственных препаратов. Путём пиноцитоза в клетки поступают питательные вещества из кровяного русла, гормоны, ферменты, лекарственные вещества.
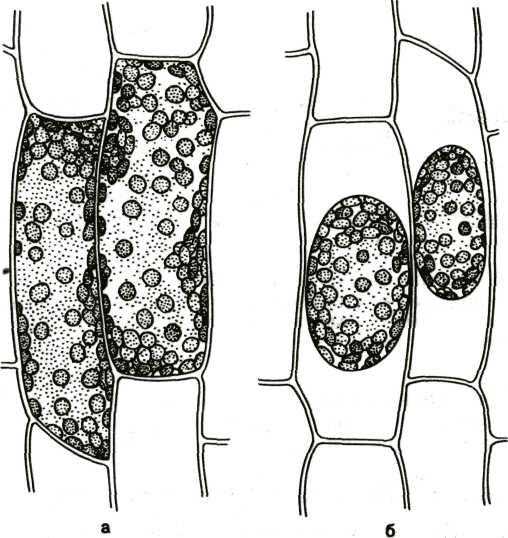
а) клетки листа элодеи б) плазмолиз в клетках листа элодеи (в 10% растворе хлорида натрия)
Суспензии, или взвеси,— мутные жидкости, частицы которых размером более 0,2 мкм. При отстаивании взвешенные частицы оседают.
Коллоидные растворы. Если частицы имеют промежуточные размеры от 0,1 до 0,001 мкм, т. е. слишком велики, чтобы образовать истинный раствор, но и слишком малы, чтобы выпасть в осадок, возникает коллоидный раствор (греч. со11а— клей). Поскольку диаметр белковых молекул превышает 0,001 мкм, белки образуют коллоидные растворы и вся протоплазма представляет собой коллоид. В коллоидных растворах на поверхностях частиц создаются огромные суммарные площади
Молекулы воды, водородными связями прочно соединены с молекулами белков. Мельчайшие частицы веществ, окружённых молекулами воды, образуют коллоидные растворы – это цитоплазма, кариоплазма, межклеточные жидкости.
Вокруг белка в коллоидном растворе образуются водные или с о л ь в а т н ы е (от лат. solvare — распускать) оболочки. Сольватная связанная вода прочно удерживается коллоидными частицами белков. Молекулы воды, создавая оболочки вокруг белков, препятствуют образованию крупных частиц. Такое состояние называется д и с п е р с н ы м
Дисперсность (степень раздробленности) обратно пропорциональна размерам коллоидных частиц
d = 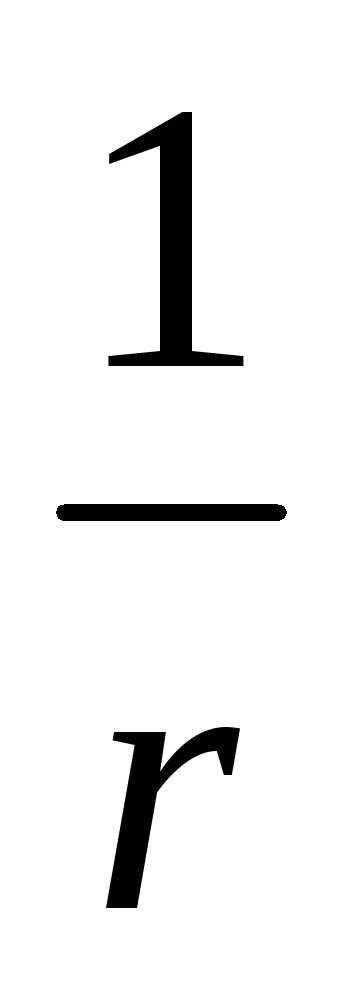 , где d—
дисперсность, r
– размер коллоидной частицы.
, где d—
дисперсность, r
– размер коллоидной частицы.
Коллоидные частицы как бы взвешены в дисперсионной среде, где создаётся огромная поверхность, на которой происходит оседание, адсорбция веществ поступающих в клетку и течение разнообразных биохимических реакций.
Коллоидные растворы бывают в двух состояниях: в виде золя (растворённый) и геля (студень, более вязкий
Гели дисперсные системы. В состоянии гель вытянутые белковые молекулы, соприкасаясь, друг с другом образуют остов из сетки, заполненный жидкостью.
Золи коллоидные р-ры с частицами, которые свободно перемещаются. Когда белковые молекулы (коллоидные частицы) расходятся, коллоид переходит в золь.
Эти процессы обратимы и в клетке совершаются непрерывно. При сокращении мышцы золь быстро переходит в гель и наоборот. При образовании псевдоподий у амёбы наблюдается переход геля в золь.
Такой переход из одного состояния в другое можно наблюдать на растворе желатина, который при нагревании — жидкий (золь), а при остывании становится студнеобразным (гель).
Коллоидное состояние определяет вязкость. Вязкость повышается, а дисперсность уменьшается, например, при повреждении клеток, размеры коллоидных частиц укрупняются, за счёт набухания и их агрегации.
ФИЗИКО—ХИМИЧЕСКИЕ СВОЙСТВА ПРОТОПЛАЗМЫ
ПОНЯТИЕ О ДИСПЕРСНЫХ СИСТЕМАХ, КОЛЛОИДНОЕ И КРИСТАЛЛИЧЕСКОЕ СОСТОЯНИЕ ПРОТОПЛАЗМЫ
Протоплазма характеризуется рядом физико-химических свойств. Это обусловлено тем, что она представляет собой сложное соединение коллоидных растворов белка и других органических веществ с истинными растворами солей и ряда неорганических соединений. Протоплазма представляет собой устойчивый гидрофильный коллоид. Коллоидным состоянием протоплазмы обусловлена ее вязкость. У большинства клеток консистенция цитоплазматического матрикса превышает вязкость воды не более чем в 5—10 раз, но в ряде случаев может быть значительно выше. Вязкость протоплазмы зависит от обменных процессов в клетках. Так, она повышается при повреждении клетки, а в яйцеклетках — после оплодотворения. Во время деления клетки обнаруживается ритмичное изменение вязкости протоплазмы. Вязкость крови меняется в зависимости от физиологического и патологического состояния организма.
Раньше единственным физическим состоянием протоплазмы считалось коллоидное. Но в последнее время обнаружено, что ряд клеточных структур представляют собой жидкие кристаллы. Жидкие кристаллы в отличие от настоящих, имеющих правильное чередование, Составляющих их молекул в трех измерениях обладают упорядоченностью лишь в двух измерениях. Жидкие, кристаллы занимают промежуточное положение между жидкостями и кристаллами. С одной стороны, они как жидкости обладают текучестью, могут сливаться друг с другом, с другой — подобно кристаллам, отличаются анизотропией, т. е. их прочность, электропроводность и ряд других свойств неодинаковы в разных направлениях. Особенности жидких кристаллов важны для понимания ряда процессов жизнедеятельности: у них иногда проявляется способность к движению, они нередко делятся почкованием. По-видимому, жидкокристаллическое состояние ряда клеточных структур обеспечивает их большую лабильность (подвижность, изменчивость).
Большой способностью к образованию жидких кристаллов обладают липиды. Жидкокристаллическая структура обнаружена в сперматозоидах, эритроцитах, клетках нервной системы и нервных волокон, палочках и колбочках сетчатки глаза.
studfiles.net
Виды растворов
3
РАСТВОРЫ
Растворы однородные смеси двух или большого числа веществ (компонентов), которые равномерно распределены в виде отдельных атомов, ионов, молекул.
Различают истинные, коллоидные растворы и суспензии.
Истинные растворы характеризуются прозрачностью, имеют малые размеры растворённых частиц, легко проходят через биологические мембраны. В зависимости от концентрации солей существует три типа растворов: изотонические; гипертонические; гипотонические;
1. И з о т о н и ч е с к и е р а с т в о р ы имеют одинаковую концентрацию солей, как и в плазме крови, и такое же осмотическое давление.
К ним относят растворы, имеющие концентрацию солей 0,9%.
Одним из таких растворов является физиологический раствор — это раствор хлорида натрия — NaCl 0,9%. В таком растворе в клетку и из клетки молекулы воды будут перемещаться в равном количестве в обе стороны.
С кл = С раствор С – концентрация солей
Н2 0
В этом растворе клетка сохраняет все жизненно важные функции, осуществляя процессы дыхания, размножения, обмена веществ.
Применение физиологического раствора.
Вводят физраствор через рот, внутривенно, внутримышечно, подкожно, в прямую кишку:
при некоторых заболеваниях – тяжелые длительные поносы, холера, неукротимая рвота, обширные ожоги хлорид натрия выделяется из организма в больших количествах, чем обычно. Также его много теряется с потом при работе в горячих цехах. В таких случаях в организме возникает его недостаточность, что сопровождается развитием ряда болезненных явлений: спазмы, судороги, нарушения кровообращения, угнетение ЦНС;
при интоксикациях, кровопотерях, обезвоживании, высокой температуре
для промывания глаз, носовой полости.
натрий хлористый является составной частью растворов применяющихся в качестве кровозамещающих (плазмозамещающих) жидкостей.
2. Г и п е р т о н и ч е с к и й р а с т в о р (2%, 5%, 10%, 15%) — это раствор в котором концентрация солей выше, чем в плазме крови.
К ним относятся растворы, содержащие более 0,9% солей. Если клетку поместить в такой раствор, то вода из клетки поступает в окружающую среду, при этом падает в клетке тургорное (осмотическое) давление, содержимое клетки сжимается, она теряет форму, происходит обезвоживание. Это явление называется — плазмолиз
. С кл < С раствор
Н2 0
Явление плазмолиза обратимое, если поместить клетку в гипотонический раствор, то в таком растворе она восстановит объем и форму Н2 0 клетка
Применяют гипертонический раствор для:
полосканий горла, для ванн, обтираний;
назначают при запорах для опорожнения кишечника.
в виде компрессов и примочек применяются при лечении гнойных ран, раны очищаются от гноя;
2 – 5% растворы используют для промывания желудка при отравлении нитратом серебра;
внутривенно используют при отёке лёгких и внутренних кровотечениях.
3. Г и п о т о н и ч е с к и й р а с т в о р, это раствор, имеющий меньшую концентрацию солей, чем в плазме крови. К ним относят ди — бидистиллированную воду, талую воду ледников. Если клетку поместить в гипотонический раствор, то в нее из раствора будет поступать вода, осмотическое давление возрастает, клетка набухает. Это явление получило название – деплазмолиз.
С кл > С раствор
Н2 0
Животные клетки, в таком растворе быстро разрушаются т.к. мембрана не выдерживает высокого осмотического давления и разрывается. Это явление называется цитолиз. Частные случаи цитолиза – разрушение эритроцитов крови – гемолиз, при этом гемоглобин выходит в плазму крови и окрашивает ее в красный цвет, такая кровь называется лаковой.
Растительные клетки в таком растворе обычно только набухают, т.к. имеют кроме цитоплазматической мембраны плотную клеточную стенку – целлюлозную оболочку. Но, если растительные клетки длительно находятся в гипотоническом растворе, то и они разрушаются.
Применяют гипотонические растворы в качестве растворителей для водорастворимых лекарственных препаратов. Путём пиноцитоза в клетки поступают питательные вещества из кровяного русла, гормоны, ферменты, лекарственные вещества.

а) клетки листа элодеи б) плазмолиз в клетках листа элодеи (в 10% растворе хлорида натрия)
Суспензии, или взвеси,— мутные жидкости, частицы которых размером более 0,2 мкм. При отстаивании взвешенные частицы оседают.
Коллоидные растворы. Если частицы имеют промежуточные размеры от 0,1 до 0,001 мкм, т. е. слишком велики, чтобы образовать истинный раствор, но и слишком малы, чтобы выпасть в осадок, возникает коллоидный раствор (греч. со11а— клей). Поскольку диаметр белковых молекул превышает 0,001 мкм, белки образуют коллоидные растворы и вся протоплазма представляет собой коллоид. В коллоидных растворах на поверхностях частиц создаются огромные суммарные площади
Молекулы воды, водородными связями прочно соединены с молекулами белков. Мельчайшие частицы веществ, окружённых молекулами воды, образуют коллоидные растворы – это цитоплазма, кариоплазма, межклеточные жидкости. В коллоидном растворе различают непрерывную фазу – дисперсионную среду (вода) и коллоидные частицы – дисперсную фазу. Коллоидной частицей протоплазмы чаще всего являются молекулы белка, т.к. их размеры соответствуют размерам коллоидных частиц.
Вокруг белка в коллоидном растворе образуются водные или с о л ь в а т н ы е (от лат. solvare — распускать) оболочки. Сольватная связанная вода прочно удерживается коллоидными частицами белков. Молекулы воды, создавая оболочки вокруг белков, препятствуют образованию крупных частиц. Такое состояние называется д и с п е р с н ы м (рассеянным, раздробленным).
Дисперсность (степень раздробленности) обратно пропорциональна размерам коллоидных частиц
d = 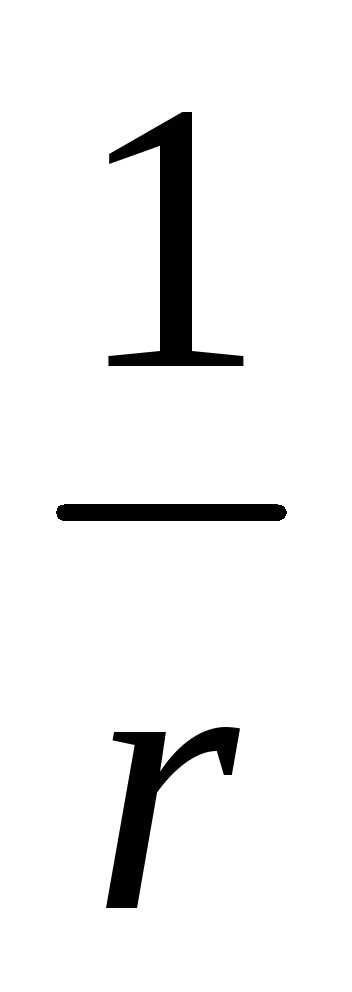 , где d—
дисперсность, r
– размер коллоидной частицы.
, где d—
дисперсность, r
– размер коллоидной частицы.
Коллоидные частицы как бы взвешены в дисперсионной среде, где создаётся огромная поверхность, на которой происходит оседание, адсорбция веществ поступающих в клетку и течение разнообразных биохимических реакций.
Коллоидные растворы бывают в двух состояниях: в виде золя (растворённый) и геля (студень, более вязкий).
Гели дисперсные системы. В состоянии гель вытянутые белковые молекулы, соприкасаясь, друг с другом образуют остов из сетки, заполненный жидкостью.
Золи коллоидные р-ры с частицами, которые свободно перемещаются. Когда белковые молекулы (коллоидные частицы) расходятся, коллоид переходит в золь.
Эти процессы обратимы и в клетке совершаются непрерывно. При сокращении мышцы золь быстро переходит в гель и наоборот. При образовании псевдоподий у амёбы наблюдается переход геля в золь.
Такой переход из одного состояния в другое можно наблюдать на растворе желатина, который при нагревании — жидкий (золь), а при остывании становится студнеобразным (гель).
Коллоидное состояние определяет вязкость. Вязкость повышается, а дисперсность уменьшается, например, при повреждении клеток, размеры коллоидных частиц укрупняются, за счёт набухания и их агрегации.
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ПРОТОПЛАЗМЫ
ПОНЯТИЕ О ДИСПЕРСНЫХ СИСТЕМАХ, КОЛЛОИДНОЕ И КРИСТАЛЛИЧЕСКОЕ СОСТОЯНИЕ ПРОТОПЛАЗМЫ
Протоплазма характеризуется рядом физико-химических свойств. Это обусловлено тем, что она представляет собой сложное соединение коллоидных растворов белка и других органических веществ с истинными растворами солей и ряда неорганических соединений. Протоплазма представляет собой устойчивый гидрофильный коллоид. Коллоидным состоянием протоплазмы обусловлена ее вязкость. У большинства клеток консистенция цитоплазматического матрикса превышает вязкость воды не более чем в 5—10 раз, но в ряде случаев может быть значительно выше. Вязкость протоплазмы зависит от обменных процессов в клетках. Так, она повышается при повреждении клетки, а в яйцеклетках — после оплодотворения. Во время деления клетки обнаруживается ритмичное изменение вязкости протоплазмы. Вязкость крови меняется в зависимости от физиологического и патологического состояния организма.
Раньше единственным физическим состоянием протоплазмы считалось коллоидное. Но в последнее время обнаружено, что ряд клеточных структур представляют собой жидкие кристаллы. Жидкие кристаллы в отличие от настоящих, имеющих правильное чередование, Составляющих их молекул в трех измерениях обладают упорядоченностью лишь в двух измерениях. Жидкие, кристаллы занимают промежуточное положение между жидкостями и кристаллами. С одной стороны, они как жидкости обладают текучестью, могут сливаться друг с другом, с другой — подобно кристаллам, отличаются анизотропией, т. е. их прочность, электропроводность и ряд других свойств неодинаковы в разных направлениях. Особенности жидких кристаллов важны для понимания ряда процессов жизнедеятельности: у них иногда проявляется способность к движению, они нередко делятся почкованием. По-видимому, жидкокристаллическое состояние ряда клеточных структур обеспечивает их большую лабильность (подвижность, изменчивость).
Большой способностью к образованию жидких кристаллов обладают липиды. Жидкокристаллическая структура обнаружена в сперматозоидах, эритроцитах, клетках нервной системы и нервных волокон, палочках и колбочках сетчатки глаза.
studfiles.net
Растворы
73
Леккия №17
РАСТВОРЫ
План
Общая характеристика растворов.
Способы выражения концентрации растворов.
Термодинамика и механизм процесса растворения.
Растворимость.
Вода как растворитель. Значение растворов в жизнедеятельности организмов
1. Общая характеристика растворов.
Растворы– это гомогенные системы переменного состава, включающие два и более компонентов. Частицы компонентов раствора распределены по его объему в виде атомов, молекул или ионов (размер частиц 0,1 – 0,5 нм).
Образование растворов, в отличие от механических смесей, сопровождается изменением энтальпии, энтропии и объема системы.
По агрегатному состоянию различают газовые, жидкие и твердые растворы. Но обычно термин растворы относится к жидким системам.
2. Способы выражения концентрации растворов.
Относительное содержание компонентов в растворе определяется его концентрацией.
Молярная концентрация– это количество вещества, содержащееся в одном литре раствора (моль/л):
Э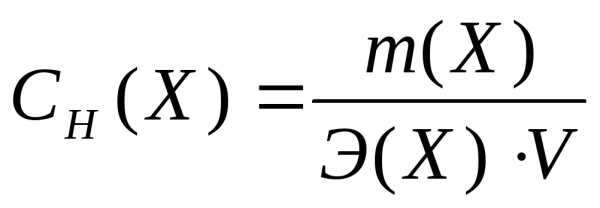 квивалентная
концентрация– это число молей
эквивалентов вещества, содержащихся в
одном литре раствора (моль/л):
квивалентная
концентрация– это число молей
эквивалентов вещества, содержащихся в
одном литре раствора (моль/л):
Эквивалент– это реальная или условная частица вещества, которая в кислотно-основной реакции эквивалентна одному иону водорода, а в окислительно-восстановительной эквивалентна одному электрону.
Масса одного моля эквивалентов называется молярной массой эквивалента вещества (Э). В разных реакциях одно и то же вещество может иметь разные эквиваленты.
Моляльная концентрация– это количество вещества, содержащееся в одном килограмме растворителя (моль/кг):
М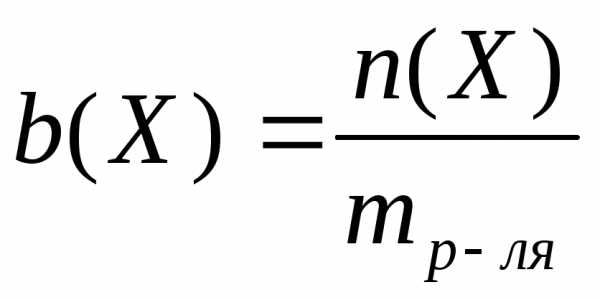 ассовая
доляравна отношению массы растворенного
вещества к массе раствора:
ассовая
доляравна отношению массы растворенного
вещества к массе раствора:
М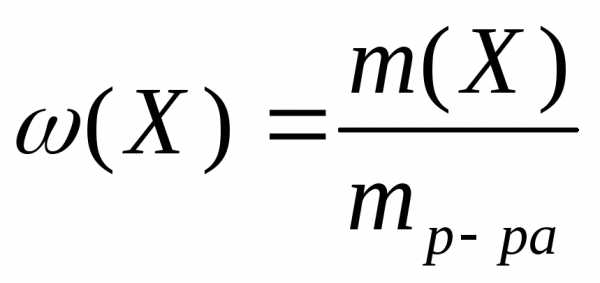 олярная
доляравна отношению количества
растворенного вещества в общему
количеству веществ в растворе:
олярная
доляравна отношению количества
растворенного вещества в общему
количеству веществ в растворе:
К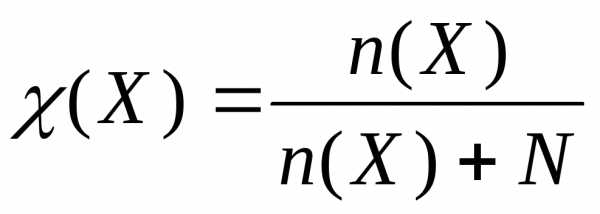 ак
правило, вещество обладает определенной
растворимостью в данном растворителе.
Подрастворимостьюпонимают
концентрацию вещества в насыщенном
растворе.
ак
правило, вещество обладает определенной
растворимостью в данном растворителе.
Подрастворимостьюпонимают
концентрацию вещества в насыщенном
растворе.
3. Термодинамика и механизм процесса растворения
Растворение – сложный физико-химический процесс, включающий три основные стадии, каждая из которых характеризуется изменениями термодинамических функций Н иS:
разрушение химических и межмолекулярных связей в растворяемом веществе (например, разрушение кристаллической решетки): Н1>0,S1>0
химическое взаимодействие частиц растворенного вещества с растворителем (сольватация): Н2<0,S2<0
равномерное распределение частиц растворенного вещества в среде растворителя путем диффузии: Н3>0,S3>0
Согласно 2-му закону термодинамики условием самопроизвольности процесса растворения является убыль энергии Гиббса:
G=H-TS< 0,
которая складывается из энтальпийного Н и энтропийногоTSфакторов.
Растворение газов в жидкостях приводит к упорядочению системы и, следовательно, сопровождается уменьшением энтропии: Sр-ния<0. Движущей силой процесса растворения в этом случае является энтальпийный фактор и растворение большинства газов является процессом экзотермическим:Нр-ния<0. Таким образом, самопроизвольное растворение газов возможно при низких температурах (|Н| > |TS|)
Растворение жидких и твердых веществ в жидкостях приводит к увеличению беспорядка в системе и увеличению энтропии: Sр-ния>0. Суммарный тепловой эффект процесса растворения определяется в основном слагаемымиН1иН2и в зависимости от их соотношения может и быть и положительным (NaCl), и отрицательным (NaOH). Растворение большинства кристаллических веществ – процесс эндотермическийНр-ния>0, так как энергия, затрачиваемая на разрушение кристаллической решетки не компенсируется энергией, выделяемой за счет сольватации. Таким образом, самопроизвольному растворению большинства твердых веществ способствуют высокие тепмературы (|Н| < |TS|).
Растворы, образование которых не сопровождается изменениями объема системы и тепловыми эффектами (V=0,Н=0), называютидеальными. Движущей силой образования идеального раствора является увеличение энтропии системы. Идеальный раствор – понятие абстрактное. Реальные системы могут лишь приближаться к идеальным. Наиболее близки к модели идеального раствора системы, в которых компоненты близки по свойствам и практически не взаимодействуют друг с другом (например, раствор толуола в бензоле). Приближаются по свойствам к идеальным бесконечно разбавленные растворы, в которых взаимодействиях сводятся к минимуму за счет низкой концентрации растворенного вещества.
4. Растворимость
Под растворимостьюпонимают концентрацию растворенного вещества в насыщенном растворе.
Растворимость выражают в тех же единицах, что и концентрацию. Часто используют коэффициент растворимости s, равный массе растворенного вещества (г) в насыщенном растворе, содержащем 100 г растворителя.
Насыщеннымназывают раствор, который находится в равновесии с избытком растворяемого вещества (Gр-ния=0). Насыщенный раствор имеет максимально возможную в данных условиях концентрацию.
Растворимость зависит:
от природы растворенного вещества и растворителя;
от температуры;
от давления;
от присутствия третьих компонентов.
Влияние природыкомпонентов на растворимость определяется принципом:подобное растворяется в подобном. Полярные растворители, например, вода, хорошо растворяют вещества с ионной связью (неорганические соли, кислоты и основания). Хорошей растворимостью в воде обладают полярные органические соединения, образующие с молекулами растворителя водородные связи (спирты, карбоновые кислоты, амины). Неполярные растворители, например, углеводороды, растворяют неполярные и малополярные соединения (жиры).
Влияние температурына растворимость зависит от теплового эффекта растворения и определяется принципом Ле Шателье. Повышению растворимости газов способствует понижение температуры, так как растворение газов – процесс экзотермический. Растворимость большинства твердых веществ и жидкостей — процесс эндотермический и возрастает при повышении температуры.
Влияние давления существенно только в том случае, если при растворении происходит значительное изменение объема системы, что наблюдается при растворении газов в жидкостях. Растворимость газов растет с увеличением давления, так как сопровождается уменьшением объема системы.
Закон Генри:
Количество газа, растворенного в определенном объеме жидкости при постоянной температуре прямо пропорционально давлению газа.
c(X) = Kгp(X)
где c(X) – молярная концентрация газа,моль/л
Kг — константа Генри, моль/лПа
p(X) – давление газа над раствором, Па
Влияние присутствия третьих компонентов.
Растворимость газов в жидкостях значительно снижается в присутствии электролитов (солей) Этот процесс называют высаливанием.
Закон Сеченова:
Растворимость газов в жидкостях в присутствии электролитов понижается.
С(X) = С0(X)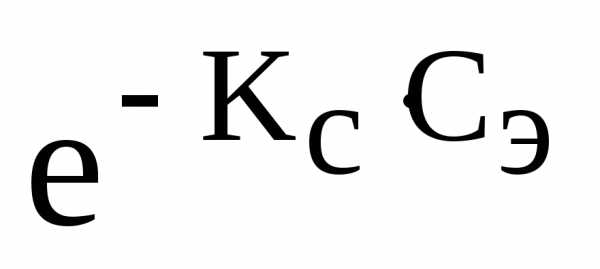
где С(X) – растворимость газа в присутствии электролита
С0(X) – растворимость газа в чистом растворителе
КС— константа Сеченова
Сэ— концентрация электролита
Биологическое значение законов Генри и Сеченова.
Изменение растворимости газов в крови при изменении давления может привести к тяжелым заболеванием. Кесонная болезнь у водолазов – проявление закона Генри. В соответствии с законом Сеченова растворимость кислорода и углекислого газа в крови зависит от концентрации электролитов, а также белков, липидов и других веществ.
5. Вода как растворитель. Значение растворов в жизнедеятельности организмов
Самым распространенным растворителем на нашей планете является вода. У животных и растительных организмов содержание воды составляет обычно более 50%, а в ряде случаев достигает 90-95%.
Вода хорошо растворяет многие ионные и полярные соединения. Такое свойство воды связано с ее высокой диэлектрической проницаемостью (= 78,5). В результате многие ионные соединения диссоциируют и отличаются высокой растворимостью в воде. Другой класс веществ, хорошо растворимых в воде, составляют полярные органические соединения (спирты, альдегиды, кетоны). Их растворимость обусловлена образованием водородных связей с молекулами воды.
Важны и другие аномальные свойства воды: высокое поверхностное натяжение, низкая вязкость, высокие температуры плавления и кипения, более высокая плотность в жидком состоянии, чем в твердом.
Вследствие высокой полярности вода вызывает гидролиз веществ (эфиров, амидов и др.). Так как вода составляет основную часть внутренней среды организма, то она обеспечивает процессы всасывания, передвижения питательных веществ и продуктов обмена в организме.
Важнейшие биологические жидкости – кровь, лимфа, моча, слюна, пот являются растворами солей, белков, углеводов, липидов в воде. Биохимические процессы в живых организмах протекает в водных растворах.
В жидких средах организма поддерживается постоянство рН, концентрации солей и органических веществ, постоянство осмотического давления. Такое постоянство называется гомеостазом. Приведенные примеры показывают, что учение о растворах представляет особый интерес для медиков.
73
studfiles.net
Виды растворов — Растворы — Аптечная технология приготовления лекарственных форм — Справочник фармацевта — Medkurs.ru
Истинные растворы характеризуются молекулярной или ионной степенью дисперсности, в растворах высокомолекулярных соединений образуются макромолекулы или их ассоциации, коллоидные растворы отличаются наличием мицелл растворенного вещества.
Истинные растворы. Такие растворы характеризуются полной гомогенностью благодаря одинаковым размерам частиц растворенного вещества и растворителя и отсутствию поверхностей раздела между ними. Истинные растворы — это однофазные дисперсные системы. Истинные растворы характеризуются большой прочностью связи между растворенной жидкостью и растворителем. Растворенная жидкость (вещество) в дальнейшем не отделяется от растворителя, остается равномерно распределенной в растворителе. Истинный раствор сохраняет гомогенность неопределенно долгое время, если только в нем не происходит никаких самопроизвольных вторичных процессов (например, гидролиза, окисления, фотосинтеза). Истинные растворы бывают ионно-дисперсными и молекулярно-дисперсными. Размер частиц в первых составляет менее 1 нм, а растворенное вещество находится в виде отдельных гидратированных ионов и молекул в равновесных количествах. Истинные растворы всегда прозрачны, они не должны содержать взвешенных частиц и осадка. Особенностью истинных растворов является то, что они гомогенны даже при рассматривании в электронный микроскоп. Компоненты, входящие в их состав, не могут быть разделены никаким способом. Истинные растворы хорошо диффундируют. К этой группе относятся растворы электролитов и неэлектролитов, таких как глюкоза, натрия хлорид, спирт, магния сульфат и т.д.
Истинные растворы высокомолекулярных соединений являются молекулярно-дисперсными системами, которые образованы дифильными макромолекулами. С одной стороны, они являются однофазными гомогенными системами (как и истинные растворы), а с другой — имеют некоторые особенности, сближающие их с коллоидными растворами (движение молекул, подобное броуновскому, малые скорости диффузии, неспособность к диализу, повышенная способность к образованию молекулярных комплексов и некоторые другие).
Коллоидные растворы. Коллоидный раствор — это гетерогенная дисперсионная система, в которой частицы растворенного вещества обладают ультрамикроскопической (коллоидной) степенью дробления. Размер частиц дисперсной фазы составляет 1—100 нм. Даже электронные иммерсионные микроскопы не всегда дают возможность визуально обнаружить частицы дисперсионной фазы коллоидных растворов. К коллоидным растворам относятся золи, размер частиц в них достаточно велик и составляет более 1/2 длины световой волны, поэтому свет не может свободно проходить через них и подвергается большему или меньшему рассеиванию. Благодаря светорассеянию золи характеризуются феноменом Тиндаля, т.е. всегда, особенно в отраженном свете, кажутся опалесцирующими, мутными. В отличие от истинных растворов золи обладают очень малым осмотическим давлением и, как следствие, высокой степенью лабильности. Элементарными единицами в золях являются сложные структурные электронейтральные агрегаты — мицеллы. Мицеллы находятся в состоянии электролитической диссоциации и состоят из массивного поливалентного иона — гранулы и соответствующего количества противоположно заряженных ионов обычного размера — противоионов. Ядро гранулы представляет собой кристаллический комплекс электронейтральных атомов или молекул. Наружная (активная) часть гранулы является адсорбционной оболочкой (сферой). Она состоит из ионов одного знака. Противоионы располагаются в интермицеллярной жидкости по соседству с гранулами и имеют некоторую возможность самостоятельного движения. Такое строение золей обусловливает и их свойства.
Как известно, под влиянием часто незначительных причин (таких как прибавление воды, растворов электролитов, нагревание, механическое встряхивание, свет, повышение температуры), а иногда и вообще самопроизвольно коллоидные растворы подвергаются разрушению — коагуляции. При коагуляции частицы растворенного вещества укрупняются, золь сильно мутнеет, превращается в суспензию, а спустя некоторое время, выпадает осадок — коагулянт. Даже при самых бережных условиях хранения золи имеют ограниченный срок существования. Особым случаем образования жидких коллоидных систем, состоящих в пограничной области между золями и суспензиями, являются тонкие мути, обозначаемые в фармацевтической практике особым термином — “турбидные микстуры” (от лат. turbide — “мутный”). Наиболее типичными случаями образования тонких мутей являются случаи разведения водными растворами многих спиртовых настоек и некоторых жидких экстрактов, а также случаи разведения водными растворителями многих спиртовых растворов, особенно имеющих концентрацию, близкую к насыщенной. Спиртовые извлечения из растительного сырья, к числу которых относятся настойки и жидкие экстракты, часто содержат сложные комплексы разнообразных компонентов растворимых и нерастворимых в воде. К числу труднорастворимых или нерастворимых в воде экстрактивных веществ, характерных для многих настоек и жидких экстрактов, относятся эфирные масла, стеарины, воск, жиры, хлорофилл и т.д. В спиртовых средах эти вещества находятся в состоянии истинного раствора. При смешивании спиртовых настоек и многих жидких экстрактов с водой концентрация спирта понижается, растворимость водонерастворимых веществ уменьшается, и наконец, они выделяются из первичного раствора, образуя гетерогенные системы. В зависимости от количества замены одного растворителя другим (спирта водой) выделение водонерастворимых веществ происходит различно и приводит к образованию систем с различной степенью дисперсности — золей, мутей, эмульсий. С технологической точки зрения желательно получить гетерогенные системы с возможно высокой степенью дисперсности водонерастворимых компонентов в жидкости. Существуют две возможности образования дисперсных систем. Первая реализуется при постепенном прибавлении к первоначальному спиртовому раствору воды, вторая — при прибавлении первоначального спиртового раствора к значительному количеству воды. Первый случай характеризуется сравнительно медленным понижением концентрации спирта, поэтому раствор водонерастворимого вещества доводится до насыщения, а затем превращается в пересыщенный раствор, из которого начинается относительно медленное выделение водонерастворимых компонентов в виде нерастворимой фазы. В таком случае в результате изменения растворяющей способности растворителя происходит процесс, напоминающий относительно упорядочную кристаллизацию. Новые порции выделяющегося вещества отмечаются преимущественно на поверхности ранее выделившихся частиц, играющих роль кристаллизационных центров. В результате образующиеся частицы дисперсной фазы увеличиваются до значительных размеров, превращаясь в довольно грубую, сравнительно быстроотслаивающуюся суспензию. Во втором случае первоначальный спиртовой раствор, попадая в избыток водного растворителя, разбавляется последним быстро. Также быстро выделяется нерастворимая фаза.
В этом случае трудно предполагать упорядоченное выделение водонепроницаемого вещества, сходного с упорядоченной кристаллизацией. Частицам, попадающим в условия резкого перепада концентрации спирта, не остается времени для роста, и они выделяются в виде тончайшей коллоидной мути, тем более тонкой, чем меньше растворимость выделяющейся дисперсной фазы в новом растворителе, образовавшемся при смешении жидкостей.
С технологической точки зрения второй случай является наиболее приемлемым. Необходимо иметь в виду, что дальнейшая судьба нерастворимой фазы сильно зависит от состава раствора, в котором она образовалась. Так как в большинстве случаев водонерастворимые вещества, содержащиеся в спиртовых извлечениях из растительных материалов, обладают кислотным характером, щелочная реакция микстуры, содержащей, например, натрия гидрокарбонат, способствует возникновению дзета-потенциала нерастворимых частиц и оказывает стабилизирующее влияние. Таким же действием обладают многие углеводы и их производные (слизи, камеди), сапонины, глицерин и другие вещества, способствующие повышению гидрофильности поверхностного слоя водонерастворимых гранул и приводящие к их гидратации.
В присутствии значительного количества нейтральных соединений устойчивость дисперсионной системы часто понижается вплоть до коагуляции. Чем выше концентрация нейтральных соединений, тем больше эта опасность. По указанной причине совершенно неправильным способом является работа, при которой сначала отмеривают нейтральное соединение (например, концентрированные растворы солей), а потом добавляют к ним настойки или жидкие экстракты. В результате возникают грубодисперсные системы.
Суспензии (suspensio) — это такие системы, которые состоят из раздробленного твердого вещества и жидкой фазы. Размер частиц в них колеблется от 0,1 до 50 мкм и более (грубодисперсные системы). Суспензии гетерогенны, но в отличие от коллоидных растворов это мутные жидкости, частицы которых видны под обычным микроскопом. Эти жидкости седиментируют, их частицы задерживаются даже крупнопористыми фильтрующими материалами. Они не склонны к диализу и диффузии.
Эмульсии (emulsus) представляют собой дисперсные системы, в которых и дисперсная фаза, и дисперсионная среда представлены взаимонерастворимыми или мало взаиморастворимыми жидкостями. Эмульсии относятся к грубодисперсным системам, в которых размер дисперсных частиц (капелек) колеблется в пределах от 1 до 150 мкм, но в некоторых случаях они бывают и более высокодисперсными.
Между тремя последними дисперсными системами нельзя провести четкую грань, что часто вызывает затруднения при прописи жидких лекарственных препаратов.
Комбинированныe дисперсныe системы включают экстракционные лекарственные формы (настои, отвары, слизи). В них действующие вещества могут находиться как в растворенном виде, так и в виде тонких суспензий и эмульсий. Кроме того, комбинированные дисперсные системы могут получаться в результате сочетаний веществ, по-разному распределяющихся в жидкой среде.
Жидкие лекарственные формы делят на препараты для наружного, внутреннего и инъекционного применения. Жидкие лекарственные формы для внутреннего применения называются микстурами (от лат. mixturae — “смешивать”), дисперсионной средой в них является только вода. Микстуры содержат три ингредиента и более. Грубые дисперсии (частицы размером 5—10 мкм), быстрооседающие и поэтому перед употреблением взбалтываемые, в аптечной практике обычно называют взбалтываемыми микстурами — mixturae agitandae (от лат. agito — “трясти”). Более тонкие растворы, по степени дисперсности приближающиеся к золям, называют микстурами мутными — mixturae turbidae (от лат. turbidus — “мутный”).
Микстуры, как правило, дозируются столовыми (15 мл), десертными (10 мл) и чайными (5 мл) ложками. Растворы для приема внутрь назначают обычно в количестве 5—15 мл, а также в каплях, которые перед употреблением разводят небольшим количеством воды или молока (масляные растворы).
Для применения раствора необходимо определить:
концентрацию раствора;
общее количество раствора.
Например, если вам выписали раствор кальция хлорида на 5 дней с таким расчетом, чтобы, применяя его внутрь по 1 ст. л., вы получали бы по 1,5 г кальция хлорида, то принимать его нужно по 1 ст. л. 4 раза в день.
Расчет концентрации раствора в процентах: 1 ст. л. — 15 мл — содержит 1,5 г вещества, т.е. раствор 10%-ный.
Расчет количества раствора. Вы будете принимать раствор по 1 ст. л. 4 раза в день в течение 5 дней, всего 20 ст. л. В 1 ст. л. —15 мл.
Следовательно, общее количество раствора — 300 мл.
При использовании внутрь лекарственных средств в каплях, достигается только приблизительная точность дозировки, так как величина капли может варьировать в зависимости от поверхностного натяжения жидкости, толщины края склянки и формы различных капельниц.
Поэтому при дозировании веществ каплями следует избегать назначения максимальных доз для ядовитых и сильнодействующих веществ, так как может произойти передозировка препарата и возникнуть отравление или аллергическая реакция.
Жидкие лекарственные формы для наружного применения назначаются в виде полосканий, примочек, растираний, клизм, капель. Дисперсионной средой в них, кроме воды, могут быть этанол, глицерин, различные масла и другие жидкости.
Помимо этого, жидкие лекарственные формы классифицируют по составу на простые (включающие одно лекарственное вещество) и сложные (в состав входит несколько ингредиентов), а также по природе жидкой среды — на водные и неводные. Более подробно об отдельных видах растворов будет рассказано ниже.
Далее по теме:
www.medkurs.ru
Понятие раствора.
Коллоидная химия
Растворы.
Растворами называют однородные системы переменного состава. Химический состав и физические свойства одного раствора во всех частях его объёма одинаковы.
В отличие от простого смешивания веществ, при растворении происходит взаимодействие между частицами, образующими раствор.
Часто для определения раствора используют понятия гомогенной и системы.
В этом случае, раствором называется гомогенная система, состоящая из двух или более компонентов.
Гомогенные и гетерогенные системы
Гомогенная система (от греч. όμός — равный, одинаковый; γένω — рождать) — однородная система, химический состав и физические свойства которой во всех частях одинаковы или меняются непрерывно, без скачков (между частями системы нет поверхностей раздела).
В гомогенной системе из двух и более химических компонентов каждый компонент распределен в массе другого в виде молекул, атомов, ионов. Составные части гомогенной системы нельзя отделить друг от друга механическим путем.
Гетерогенная система (от греч. έτερος — разный; γένω — рождать) — неоднородная система, состоящая из однородных частей (фаз), разделённых поверхностью раздела.
Растворы могут существовать в трёх агрегатных состояниях – твёрдом, жидком и газообразном (парообразном). Примерами твёрдых растворов могут служить некоторые сплавы металлов, например сплав золота и меди, газообразных – воздух.
Наиболее важный вид растворов – жидкие растворы.
Растворы имеют чрезвычайно важное значение в жизни человека. Так, процессы усвоения пищи человеком и животными связаны с переводом питательных веществ в раствор. Растворами являются все важнейшие физиологические жидкости (кровь, лимфа и т.д.).
Растворители
Всякий раствор состоит из растворённых веществ и растворителя, т.е. среды, в которой эти вещества равномерно распределены в виде молекул и ионов.
Обычно растворителем считают тот компонент, который в чистом виде существует в том же агрегатном состоянии, что и полученный раствор. Например, в случае водного раствора соли растворителем является вода.
Если же оба компонента до растворения находились в одинаковом агрегатном состоянии (например, спирт и вода), то растворителем считается компонент, находящийся в большем количестве.
Истинные и коллоидные растворы
В растворах вещества могут находиться в различных степенях дисперсности (т.е. раздробленности). Величина частиц служит важным признаком, обуславливающим многие физикохимические свойства растворов.
По величине частиц растворы делятся на:
1. Истинные растворы (размер частиц меньше 1 мкм) и
2. Коллоидные растворы (размер частиц от 1 до 100 мкм).
Смеси с частицами размером более 100 мкм образуют взвеси: суспензии и эмульсии.
Истинные растворы могут быть ионными или молекулярными в зависимости от того, диссоциирует ли растворённое вещество на ионы или остаётся в недиссоциированном состоянии в виде молекул.
Коллоидные растворы резко отличаются по свойствам от истинных растворов. Они гетерогенны, так как имеют поверхность раздела между фазами – растворённым веществом (дисперсной фазой) и растворителем (дисперсионной средой).
Растворы высокомолекулярных соединений: белков, полисахаридов, каучука обладают свойствами как истинных, так и коллоидных растворов и выделяются в особую группу.
Растворы, механические смеси и химические соединения
Однородность растворов делает их очень сходными с химическими соединениями.
Химическое соединение — сложное вещество, состоящее из химически связанных атомов двух или нескольких элементов.
Раствор это не одно химическое соединение, а как минимум два смешанных соединения. В отличие от простого смешивания веществ, при растворении происходит взаимодействие между частицами, образующими раствор.
Выделение теплоты при растворении некоторых веществ тоже указывает на химическое взаимодействие между растворителем и растворяемым веществом.
Отличие растворов от химических соединений состоит в том, что состав раствора может изменяться в широких пределах. Кроме того, в свойствах раствора можно обнаружить многие свойства его отдельных компонентов, чего не наблюдается в случае химического соединения.
Непостоянство состава растворов приближает их к механическим смесям.
Механическая смесь — физико-химическая система, в состав которой входят два или несколько химических соединений (компонентов). В смеси исходные вещества включены неизменными. При смешивании не возникает никакое новое вещество.
От механических смесей растворы резко отличаются своею однородностью. Таким образом, растворы занимают промежуточное положение между механическими смесями и химическими соединениями.
Процесс растворения
Растворение кристалла в жидкости протекает следующим образом.
Когда вносят кристалл в жидкость, в которой он может растворяться, от поверхности его отрываются отдельные молекулы. Последние благодаря диффузии равномерно распределяются по всему объёму растворителя.
Отделение молекул от поверхности твёрдого тела вызывается, с одной стороны, их собственным колебательным движением, а сдругой – притяжением со стороны молекул растворителя.
Этот процесс должен был бы продолжаться до полного до полного растворения любого количества кристаллов, если бы не происходил обратный процесс – кристаллизация. Перешедшие в раствор молекулы, ударяясь о поверхность ещё не растворившегося вещества, снова притягиваются к нему и входят в состав его кристаллов.
Понятно, что выделение молекул из раствора будет идти тем быстрее, чем больше концентрация раствора. А так как последняя по мере растворения вещества увеличивается, то, наконец наступает такой момент, когда скорость растворения становится равной скорости кристаллизации. Тогда устанавливается динамическое равновесие, при котором в единицу времени растворяется и кристаллизуется одинаковое число молекул.
Раствор, находящийся в равновесии с растворяющимся веществом, называется насыщенным раствором.
Концентрация растворов
Насыщенными растворами приходится пользоваться сравнительно редко. В большинстве случаев употребляются растворы ненасыщенные, т.е. с меньшей концентрацией растворённого вещества, чем в насыщенном растворе.
Концентрацией раствора называется количество растворённого вещества, содержащееся в определённом количестве раствора или растворителя.
Растворы с большой концентрацией растворённого вещества называются концентрированными, с малой – разбавленными.
Концентрацию раствора можно выражать по разному:
1. В процентах растворённого вещества по отношению ко всему количеству раствора.
2. Числом грам-молекул растворённого вещества, содержащегося в 1 литре раствора.
3. Числом грамм-молекул растворённого вещества, содержащегося в 1000 г растворителя и т.д.
Растворимость
Растворимостью называется способность вещества растворяться в том или ином растворителе.
Мерой растворимости вещества при данных условиях служит концентрация его насыщенного раствора.
Растворимость различных веществ колеблется в широких пределах.
- Если в 100 граммах воды растворяется более 10 г вещества, то такое вещество принято называть хорошо растворимым.
- Если растворяется менее 1 г вещества – малорастворимым.
- Если в раствор переходит менее 0,01 г вещества, то такое вещество называют практически нерастворимым.
Принципы, позволяющие предсказать растворимость вещества, пока не известны. Однако, обычно вещества, состоящие из полярных молекул, и вещества с ионным типам связи лучше растворяются в полярных растворителях (вода, спиры, жидкий амиак), а неполярные вещества – в неполярных растворителях (бензол, сероуглерод).
Растворение большинства твёрдых тел сопровождается поглощением теплоты. Это объясняется затратой значительного количества энергии на разрушение кристаллической решётки твёрдого тела, что обычно не полностью компенсируется энергией, выделяющейся при образовании гидратов (сольватов).
Как правило, повышение температуры должно приводить к увеличению растворимости твёрдых тел.
xn—-7sbb4aandjwsmn3a8g6b.xn--p1ai
Истинные растворы — это что такое? Свойства и состав
В природе практически не встречаются чистые вещества. В основном они представлены в виде смесей, которые способны образовывать гомогенные либо гетерогенные системы.

Особенности истинных растворов
Истинные растворы — это разновидность дисперсных систем, имеющих большую прочность между дисперсионной средой и дисперсной фазой.
У любого химического вещества можно получить кристаллы разных размеров. В любом случае у них будет одинаковое внутреннее строение: ионная либо молекулярная кристаллическая решетка.
Растворение
В процессе растворения в воде крупинок хлорида натрия и сахара происходит образование ионного и молекулярного раствора. В зависимости от степени раздробленности, вещество способно находиться в виде:
- видимых макроскопических частиц, размер которых больше 0,2 мм;
- микроскопических частиц, имеющих размер меньше 0,2 мм, уловить их можно только с помощью микроскопа.
Истинные и коллоидные растворы отличаются между собой размером частиц растворяемого вещества. Невидимые в микроскоп кристаллы называют коллоидными частицами, а получаемое состояние именуют коллоидным раствором.

Фаза раствора
Во многих случаях истинные растворы — это раздробленные (дисперсные) системы гомогенного вида. В них присутствует сплошная непрерывная фаза – дисперсионная среда, и раздробленные частицы определенной формы и размера (дисперсная фаза). Чем отличаются коллоидные растворы от истинных систем?
Основное различие состоит в размерах частиц. Коллоидно-дисперсные системы считают гетерогенными, так как в световом микроскопе невозможно обнаружить границу раздела фаз.
Истинные растворы — это тот вариант, когда в окружающей среде вещество представлено в виде ионов либо молекул. Они относятся к однофазным гомогенным растворам.
В качестве обязательного условия образования дисперсных систем рассматривается взаимное растворение дисперсионной среды и диспергируемого вещества. К примеру, хлорид натрия и сахароза нерастворимы в бензоле и керосине, поэтому в таком растворителе не будут образовываться коллоидные растворы.
Классификация дисперсных систем
Как делятся дисперсные системы? Истинные растворы, коллоидные системы отличаются по нескольким параметрам.
Существует подразделение дисперсных систем по агрегатному состоянию среды и дисперсной фазы, образованию либо отсутствию взаимодействия между ними.
Характеристики
Существуют определенные количественные характеристики дисперсности вещества. В первую очередь выделяют степень дисперсности. Эта величина обратна размеру частиц. Она характеризует то количество частичек, которое можно разместить в ряд на расстоянии одного сантиметра.
В том случае, когда все частицы обладают одинаковыми размерами, образуется монодисперсная система. При неодинаковых частицах дисперсной фазы образуется полидисперсная система.
С повышением дисперсности вещества у него повышаются процессы, которые происходят в межфазовой поверхности. Например, возрастает удельная поверхность дисперсной фазы, растет физико-химическое воздействие среды на границе раздела двух фаз.

Варианты дисперсных систем
В зависимости от того, в какой фазе будет находиться растворяемое вещество, выделяют разные варианты дисперсных систем.
Аэрозоли – дисперсные системы, в которых дисперсная среда представлена в газообразном виде. Туманы — это аэрозоли, имеющие жидкую дисперсную фазу. Дым и пыль образуются твердой дисперсной фазой.
Пены являются дисперсией в жидкости газообразного вещества. Жидкости в пенах вырождаются до пленок, которые разделяют пузырьки газа.
Эмульсиями называют дисперсные системы, где одна жидкость распределяется по объему другой, не растворяясь в ней.
Суспензии или взвеси — это низкодисперсные системы, в которых твердые частицы находятся в жидкости. Коллоидные растворы или золи при водной дисперсной системе называют гидрозолями.
В зависимости от наличия (отсутствия) между частицами дисперсной фазы выделяют свободнодисперсные или связнодисперсные системы. К первой группе относятся лиозоли, аэрозоли, эмульсии, суспензии. В таких системах отсутствуют контакты между частицами и дисперсной фазой. Они без ограничений передвигаются в растворе под действием силы тяжести.
Связнодисперсные системы возникают в случае контакта частиц с дисперсной фазой, в результате которых образуются структуры в виде сетки либо каркаса. Такие коллоидные системы называют гелями.
Процесс гелеобразования (желатинирования) представляет собой превращение золя в гель, основанный на понижении устойчивости исходного золя. Примерами связнодисперсных систем являются суспензии, эмульсии, порошки, пены. К ним также можно отнести почву, образованную в процессе взаимодействия органических (гумусных) веществ и почвенных минералов.
Капиллярно-дисперсные системы отличаются сплошной массой вещества, пронизывающей капилляры и поры. Ими считают ткани, разные мембраны, дерево, картон, бумагу.
Истинные растворы — это гомогенные системы, состоящие из двух компонентов. Они могут существовать в разных по агрегатному состоянию растворителях. Растворителем считают вещество, взятое в избытке. Компонент, который берут в недостаточном количестве, считается растворенным веществом.

Особенности растворов
Твердые сплавы тоже являются растворами, в которых в роли дисперсной среды и компонента выступают различные металлы. С практической точки зрения особый интерес представляют такие жидкие смеси, в которых жидкость выступает растворителем.
Из многочисленных неорганических растворителей особый интерес представляет вода. Практически всегда истинный раствор образуется при смешивании с водой частичек растворяемого вещества.
Среди органических соединений прекрасными растворителями являются следующие вещества: этанол, метанол, бензол, четыреххлористый углерод, ацетон. Благодаря хаотичному движению молекул или ионов растворяемого компонента происходит частичный переход их в раствор, образование новой однородной системы.
Вещества отличаются по способности образования растворов. Одни могут смешиваться друг с другом в неограниченных количествах. Примером служит растворение в воде кристаллов поваренной соли.
Суть процесса растворения с точки зрения молекулярно-кинетической теории заключается в том, что после внесения в растворитель кристаллов поваренной соли происходит диссоциация его на катионы натрия и анионы хлора. Заряженные частицы совершают колебательное движение, соударения с частицами самого растворителя приводят к переходу ионов в растворитель (связыванию). Постепенно к процессу подключаются и другие частицы, разрушается поверхностный слой, кристалл соли растворяется в воде. Диффузия позволяет распределять частицы вещества по объему растворителя.

Виды истинных растворов
Истинный раствор — это система, которая подразделяется на несколько видов. Существует классификация таких систем на водные и неводные по виду растворителя. Их также классифицируют по варианту растворенного вещества на щелочи, кислоты, соли.
Есть различные виды истинных растворов по отношению к электрическому току: неэлектролиты, электролиты. В зависимости от концентрации растворяемого вещества они могут быть разбавленными либо концентрированными.
Истинные растворы низкомолекулярных веществ с термодинамической точки зрения делят на реальные и идеальные.
Такие растворы могут быть ионно-дисперсными, а также молекулярно-дисперсными системами.

Насыщенность растворов
В зависимости от того, какое количество частиц переходит в раствор, существуют пересыщенные, ненасыщенные, насыщенные растворы. Раствор представляет собой жидкую либо твердую гомогенную систему, которая состоит из нескольких компонентов. В любой подобной системе обязательно присутствует растворитель, а также растворенное вещество. При растворении некоторых веществ наблюдается выделение тепла.
Подобный процесс подтверждает теорию растворов, согласно которой, растворение рассматривается как физико-химический процесс. Существует подразделение процесса растворимости на три группы. Первую составляют те вещества, которые способны растворяться в количестве от 10 г в 100 г растворителя, их именуют хорошо растворимыми.
Малорастворимыми считают вещества, если меньше 10 г растворяется в 100 г компонента, остальные называют нерастворимыми.
Заключение
Системы, состоящие из разных по агрегатному состоянию, размерам частиц, необходимы для нормальной жизнедеятельности человека. Истинные, коллоидные растворы, рассмотренные выше, используют для изготовления лекарственных препаратов, создания продуктов питания. Имея представление о концентрации растворенного вещества, можно самостоятельно приготовить необходимый раствор, например, этилового спирта или уксусной кислоты, для различных целей в повседневной жизни. В зависимости от того, в каком агрегатном состоянии находятся растворяемое вещество и растворитель, получаемые системы имеют определенные физические и химические характеристики.
fb.ru
