Ветровлагозащитная мембрана Изоспан А
СодержаниеПрактически каждое здание нуждается в качественном утеплении, пускай это даже теплоизоляция для теплого пола водяного образца. Это настоящая аксиома в строительном мире. Дома необходимо утеплять, так как изначально их конструкции не способны выдерживать перепады температур и быстро промерзают в холодное время года.
Однако мало просто отделать стены утеплителем. Нужно создать настоящий теплоизоляционный пирог, немаловажную роль в котором играет ветровлагозащитная или просто влагозащитная пленка.
Полная линейка продукции Изоспан
Мы же сейчас разберемся в том, что же собой представляет влагозащитная пленка на примере продукции компании Изоспан. В особенности товаров Изоспан А и Изоспан АМ вкупе с звукоизоляционными материалами Изовер.
1 Особенности пленки Изоспан
Компания Изоспан занимается производством изоляционных материалов уже очень давно. На рынке они за все время своего существования успели зарекомендовать себя с наилучшей стороны.
Основная линейка товаров от этого производителя являет собой специальную защитную пленку. Существует пленка Изоспан А, Изоспан Б, Изоспан С и т.д. Разница между этими материалами есть и на нее нужно обращать внимание.
Хоть стоит отметить интересный факт, визуально отличий между пленками модели А и С практически не наблюдается. Размеры у них тоже одинаковы.
Остается уповать на технические характеристики и саму сферу назначения. Если же оценивать изоляцию со стороны ее свойств, от отличия между разными материалами становятся очевидны.
к меню ↑
1.1
Различия между материаламиВетер – это очень серьезный раздражитель. В отличие от обычной влаги или пара, он постоянно воздействует на окружающие конструкции. А современные утеплители (та же минвата или пенопласт) не имеют достаточной плотности, поэтому подвергаются нагрузкам извне.
А современные утеплители (та же минвата или пенопласт) не имеют достаточной плотности, поэтому подвергаются нагрузкам извне.
Медленно, но уверенно ветер, будет подтачивать прочность материала, пока полностью его не разрушит.
С влагой ситуация обстоит иначе, но это наверняка и так всем ясно. Влагозащитная пленка является настоящей необходимостью. Ведь именно влагозащитная изоляция позволяет ограничить утеплитель от попадания внутрь него воды.
А воду, между прочим, удалить из уже установленных плит изоляции крайне сложно. Если же конструкции у вас невентилируемые, то и вовсе невозможно. Как видите, ветровлагозащитная пленка выполняет крайне полезные функции.
Влагозащитная мембрана Изоспан А в упаковке
Пленка влагозащитная мембрана Изоспан В как и Изоспан АМ уже концентрируется на немного других задачах. Здесь основной упор делается на защиту теплоизоляции от проникновения пара. Толщина у нее, как правило, меньше, но и стоимость тоже существенно ниже.
Многих интересует вопрос, есть ли разница между изоляцией Изоспан А и АМ. И действительно, если глядеть только на технические свойства, то материалы кажутся идентичными.
Однако определенные различия все же имеются. Достаточно посмотреть в сертификат продукции, где указаны полные технические характеристики и назначение материала.
Изначально мембрана Изоспан А имеет большую плотность и она дополнительно защищена от повреждений во время монтажа. Поэтому производитель рекомендует использовать ее преимущественно для отделки стен. В особенности для работы в вентилируемых каркасах утепления.
А вот Изоспан АМ чуть слабее в плане прочности, что вынуждает пользователя применять ее в местах с меньшей нагрузкой. В итоге практически идеально модель АМ подходит для отделки кровли.
к меню ↑
1.2 Свойства и параметры
Теперь стоит оценить непосредственно технические характеристики изоляционных мембран Изоспан, а также ее интересные нюансы. Но для начала отметим, что все описываемые дальше свойства являются таковыми, когда вы пользуетесь продукцией, что получила сертификат.
Но для начала отметим, что все описываемые дальше свойства являются таковыми, когда вы пользуетесь продукцией, что получила сертификат.
Сертификат соответствия имеется у всей продукции компании Изоспан. Поэтому вы вправе при покупке требовать сертификат у продавца, тем самым желая убедиться в том, что вам не пытаются подсунуть подделку.
Сертификат соответствия выдается государственными органами и содержит в себе информацию о товаре, знак его качества и т.д. Также сертификат позволяет убедиться в том, что заявленные на упаковке ингредиенты в мембране действительно присутствуют.
Казалось бы, зачем такая излишняя осторожность? Ведь это всего лишь изоляция. Но на самом деле вам надо понимать, что изоляция имеет не меньший вес в конструкции, чем тот же утеплитель.
Шероховатая поверхность мембраны Изоспан АМ
Можно закупить дорогущий утеплитель из минваты и отделать им все конструкции, надеясь на чудо. Но если вами не будет установлена хотя бы обычная ветровлагозащитаная мембрана, то уже через несколько лет могут начаться серьезные проблемы.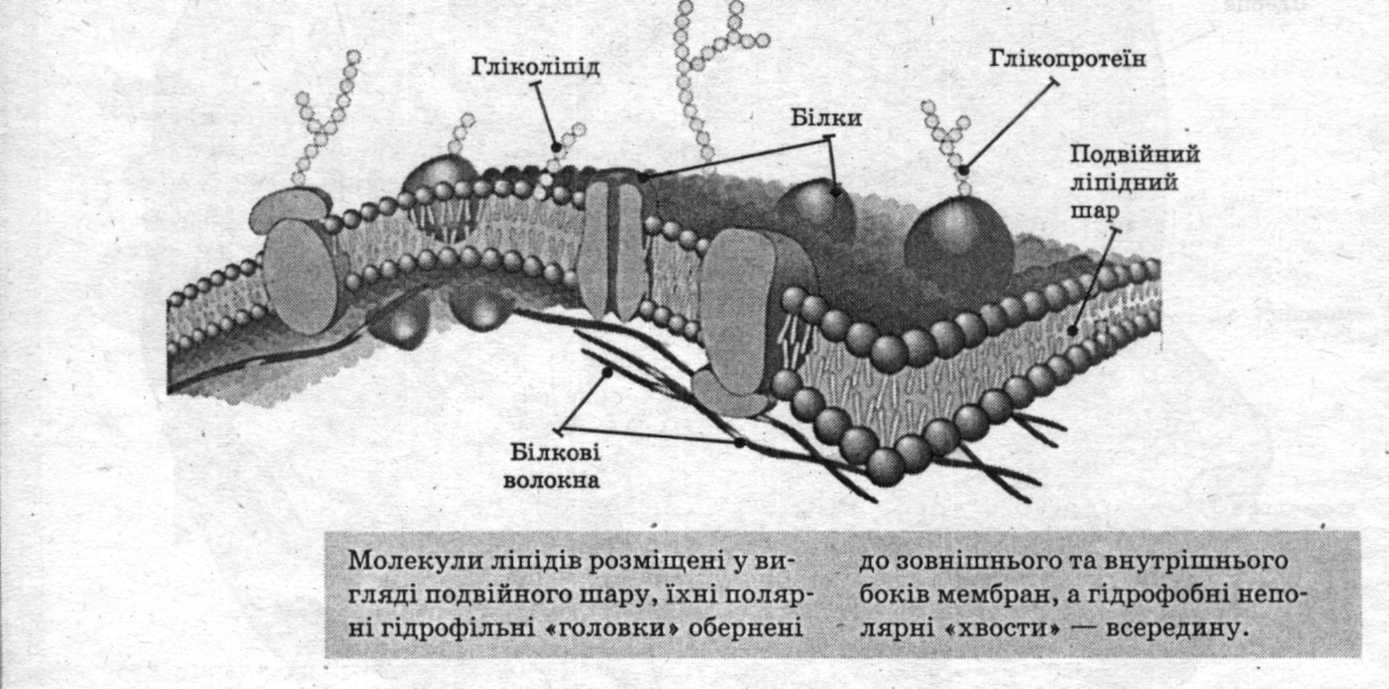
к меню ↑
2 Особенности производства
Ветровлагозащитная мембрана производится на фирменном оборудовании в цехах компании Изоспан. Ее создают из плотного полипропилена. Причем полимер используется смешанный с кучей химических компонентов как в звукоизоляционных материалах Изовер.
Только не стоит бояться, ничего вредного в нем нет. Эти компоненты только способствуют укреплению материала и его долговечности. Так, мембрана Изоспан модели АМ из-за наличия в ней отдельного класса полимеров имеет куда более высокую плотность, чем у продукции конкурентов.
А ведь модель АМ – это далеко не самый прочный образец из линейки Изоспан.
Еще один важный момент – двухслойное покрытие пленки. Вернее, наличие у нее двух сторон. То есть мембрана имеет разное покрытие на каждой стороне.
Одна сторона – влагоотталкивающая. Монтируется наружу от утеплителя. Она гладкая и очень прочная, предназначается для защиты от ветра и влаги. Ветер такой полимер продуть не в состоянии, а вода просто стекает по нему вниз, где убирается по дренажным отводам.
Вторая сторона – влагозадерживающая, шероховатая. Именно ее направляют лицом к утеплителю. Ее задача заключается в сборе конденсата, ведь мембрана паропроницаема. На шероховатой поверхности конденсат задерживается, а затем выветривается, не оказывая влияния на утеплитель внутри.
Собственно, в этом и заключаются уникальные характеристики пленки Изоспан. С одной стороны она полностью защищает утеплитель от влаги. С другой же задерживает ее, не давая стечь внутрь теплоизоляции.
Такое сочетание смогло завоевать доверие строителей по всему миру. Лучше только отражающие теплоизоляционные материалы.
к меню ↑
2.1 Порядок монтажа
Рассмотрим порядок укладки мембраны. Стоит заметить, что для каждой конструкции он свой. В отличие от паронепроницаемой пленки, ветровлагозащитная мембрана паропроницаема, то есть она не блокирует пар.
Она скорее выполняет функции внешней изоляции. Своеобразного ограничителя и внешнего ограждения для плит утеплителя.
Пример монтажа пленки Изоспан на кровле
Соответственно и монтировать ее нужно в определенном месте.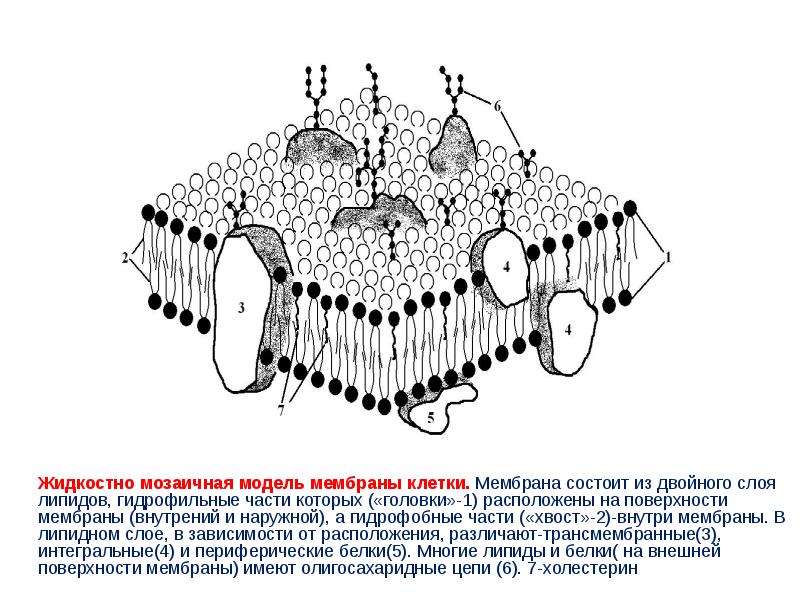
Изначально любой теплоизоляционный порог состоит из следующих слоев:
- Основание;
- Пароизоляция;
- Утеплитель;
- Гидроизоляция;
- Обрешетка;
- Лицевой материал.
Именно на месте гидроизоляции Изоспан А и монтируют. Но тут тоже важно отметить несколько нюансов.
Например, при отделке фасадов материал монтируют непосредственно на утеплитель, затем прикрывая специальными планками либо не фиксируя каркасом вообще. Можно обойтись и основательным фиксированием с помощью строительного степлера.
А вот отделка кровли уже проходит по немного другой процедуре. Тут мембрану надо ставить сразу под полость стропил или панели кровельной конструкции. Затем уже укладывают каркас или сам утеплитель.
к меню ↑
3 Технология монтажа
Укладывают влагозащитную мембрану по простой процедуре. Тут важно только качественно заделать все стыки и убедиться в том, что в материале не осталось отверстий.
Этапы работы:
- Распаковываем пленку.

- При необходимости нарезаем.
- Выполняем укладку изоляции, начиная с нижнего уровня конструкции.
- Монтируем каждый уровень над предыдущим, соблюдая нахлестывание.
- Закрепляем пленку степлером.
- Проклеиваем все стыки защитной лентой.
Не стоит экономить на мембране. Старайтесь перекрывать каждый следующий слой пленкой с длиной не меньше 20 см. Это позволит вам полностью избавиться от возможности протекания конструкций.
Использование гидроизоляции Изоспан А на стене вагончика
Поверх влагозащитной мембраны рекомендуется монтировать направляющие планки толщиной в 2-3 см. Такие планки обрабатывают антисептиком и антипиренами. Желательно монтировать их аккуратно, чтобы случайно не повредить изоляцию.
Поверх планок уже набивают лицевое покрытие. Таким образом, вам удастся организовать что-то типа вентилируемого зазора, который будет способствовать испарению жидкости на мембране.
Однако надо отметить, что в случае работы с изоляцией Изоспан А или АМ соблюдение наличия нормально воздушного зазора не всегда требуется в полной мере. Очень часто без него можно и обойтись. Но лучше, конечно, такими решениями не злоупотреблять, разве что вы живете в очень сухом климате.
Очень часто без него можно и обойтись. Но лучше, конечно, такими решениями не злоупотреблять, разве что вы живете в очень сухом климате.
к меню ↑
3.1 Инструкция по применению мембраны Изоспан А (видео)
Мембрана ветро-влагозащитная Изоспан А 70кв.м
Описание
Ветрозащитная паропроницаемая мембрана. Назначение: 1. Защищает утеплитель и внутренние элементы стен от осадков, проникающих под наружную обшивку. 2. Дополнительно фиксирует утеплитель в конструкции. 3. Выполняет функцию ветрозащиты, препятствуя конвективному движению воздуха через теплоизоляцию, снижая теплопотери. 4. В конструкции межкомнатных перегородок предотвращает проникновение частиц утеплителя во внутреннее пространство здания. 5. Благодаря паропроницаемости не препятствует выходу водяных паров из утеплителя. Применение: Каркасные стены, стены с наружным утеплением, вентилируемые фасады, межкомнатные перегородки, цокольные перекрытия. Особенности изоспана А: 1. Высокая плотность. 2. Высокая паропроницаемость.
Благодаря паропроницаемости не препятствует выходу водяных паров из утеплителя. Применение: Каркасные стены, стены с наружным утеплением, вентилируемые фасады, межкомнатные перегородки, цокольные перекрытия. Особенности изоспана А: 1. Высокая плотность. 2. Высокая паропроницаемость.
В наличии 3346 ₽
Под заказ: до 14 рабочих дней 3346 ₽
Характеристики
- Размеры
Длина:
43750 мм
Ширина:
1600 мм
- Вес, Объем
Вес:
7.5 кг
- Другие параметры
Паропроницаемость не менее, г м2сут:
3500
Производитель:
Разрывная нагрузка прод.попер. не менее,:
190/139
Состав:
100% полипропилен
Срок хранения(мес):
18
Страна происхож.:
Россия
Тип:
гидроизоляция; ветрозащита; пароизоляция
Торговая марка:
УФ-стабильность, мес.
 :
:3-4
Водоупорность не менее, мм.вод.ст.:
330
Характеристики
Торговый дом «ВИМОС» осуществляет доставку строительных, отделочных материалов и хозяйственных товаров. Наш автопарк — это более 100 единиц транспортных стредств. На каждой базе разработана грамотная система логистики, которая позволяет доставить Ваш товар в оговоренные сроки. Наши специалисты смогут быстро и точно рассчитать стоимость доставки с учетом веса и габаритов груза, а также километража до места доставки.
Заказ доставки осуществляется через наш колл-центр по телефону: +7 (812) 666-66-55 или при
заказе товара с доставкой через интернет-магазин. Расчет стоимости доставки производится
согласно тарифной сетке, представленной ниже. Точная стоимость доставки определяется после
согласования заказа с вашим менеджером.
Расчет стоимости доставки производится
согласно тарифной сетке, представленной ниже. Точная стоимость доставки определяется после
согласования заказа с вашим менеджером.
Уважаемые покупатели! Правила возврата и обмена товаров, купленных через наш интернет-магазин регулируются Пользовательским соглашением и законодательством РФ.
ВНИМАНИЕ! Обмен и возврат товара надлежащего качества возможен только в случае, если указанный товар не был в употреблении, сохранены его товарный вид, потребительские свойства, пломбы, фабричные ярлыки, упаковка.
Доп. информация
Цена, описание, изображение (включая цвет) и инструкции к
товару Мембрана ветро-влагозащитная Изоспан А 70кв.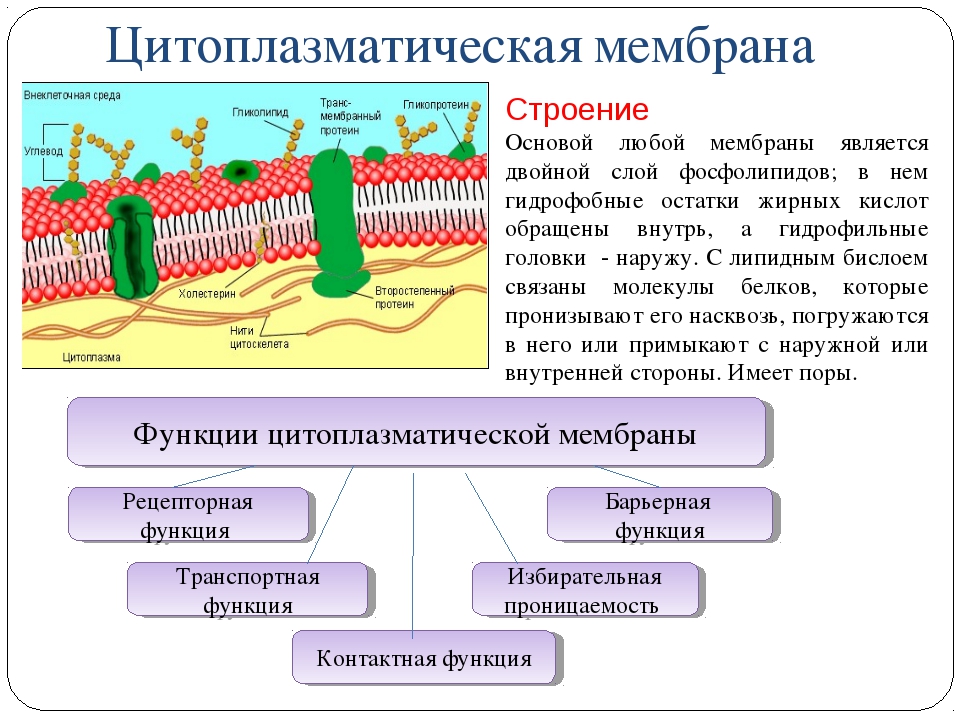 м на сайте носят информационный
характер и не являются публичной офертой, определенной п.2 ст. 437 Гражданского
кодекса Российской федерации. Они могут быть изменены производителем без предварительного
уведомления и могут отличаться от описаний на сайте производителя и реальных характеристик
товара. Для получения подробной информации о характеристиках данного товара обращайтесь
к сотрудникам нашего отдела продаж или в Российское представительство данного
товара, а также, пожалуйста, внимательно проверяйте товар при покупке.
м на сайте носят информационный
характер и не являются публичной офертой, определенной п.2 ст. 437 Гражданского
кодекса Российской федерации. Они могут быть изменены производителем без предварительного
уведомления и могут отличаться от описаний на сайте производителя и реальных характеристик
товара. Для получения подробной информации о характеристиках данного товара обращайтесь
к сотрудникам нашего отдела продаж или в Российское представительство данного
товара, а также, пожалуйста, внимательно проверяйте товар при покупке.
Купить Мембрана ветро-влагозащитная Изоспан А 70кв.м в магазине Санкт-Петербург вы можете в интернет-магазине «ВИМОС».
Статьи по теме
Мембрана PentaIzol А ветро-влагозащитная паропроницаемая 15 кв.
 м
мПодробное описание
Артикул № 4124871
Мембрана PentaIzol А ветро-влагозащитная паропроницаемая — прочная и легкая по весу пленка с высокими физико-механическими характеристиками. Материал закрепляется с внешней стороны утеплителя под наружной облицовкой стены или кровельным покрытием.
Преимущества
— Использование мембраны позволяет сохранить термозащитные свойства утеплителя, а также существенно продлевает срок его службы.
— Листы имеют влагоотталкивающую и антиконденсатную поверхность, благодаря чему удерживают образовавшиеся капли, не давая им повредить утеплитель.
— Изделие выполнено из экологически безопасных материалов.
— Минимальный срок эксплуатации — 50 лет.
Область применения
Мембрана PentaIzol А используется для защиты вентилируемых фасадов, кровель и стен с наружным утеплением. Рекомендуемый угол наклона крыши — не менее 35 градусов. Изделие является промежуточным слоем между утеплителем и внешней облицовкой (черепица, битумная плита, сайдинг, вагонка и пр. ).
).
Торговая марка PentaIzol принадлежит российской компании ООО Лига, которая работает на рынке с 2003 года. В широком ассортименте представлены вспомогательные строительные товары — изоляции, сетки, армированная пленка, скотч и многое другое. Продукция изготавливается согласно требованиям ГОСТ, имеет необходимые сертификаты качества и безопасности.
Технические характеристики
| Общие параметры | |
|---|---|
| Вид: | Рулоны |
| Размеры и вес (брутто) | |
|---|---|
| Вес: | 1,43 кг |
| Высота: | 160,0 см |
| Ширина: | 9,5 см |
| Глубина: | 9,5 см |
| Дополнительная информация | |
|---|---|
| Страна производства: | Россия |
| Срок службы: | 600 месяцев |
| Срок годности: | 24 месяца |
| Гарантийный срок: | 24 месяца |
Все, что нужно знать о мембранах и мембранной одежде
Саша и Лариса в куртках Bergans с мембраной Dermizax 20000 mm
Мембраны бывают разными: поровые, беспоровые, волоконные, гибридные и пр… По материалу они бывают: полиуретановые, тетрафторэтиленовые и, опять же, гибридные. Еще они бывают гидрофобными и гидрофильными. А еще они очень разные по показателям водонепроницаемости и паропроницаемости (дышимости). И пусть магическое слово «мембрана» не сбивает вас с толку.
Еще они бывают гидрофобными и гидрофильными. А еще они очень разные по показателям водонепроницаемости и паропроницаемости (дышимости). И пусть магическое слово «мембрана» не сбивает вас с толку.
Водонепроницаемость измеряется в мм водяного столба. Например, 20 000 мм. Меньше меня лично не интересует. Больше – очень хорошо.
Паропроницаемость, в просторечии, дышимость. Сразу скажу, что существует множество тестов: одни меряют, насколько мембрана мешает пару выходить — этот показатель, RET (resistance evaporative thermique), будет выражен в цифрах 1, 2,3, 4, и чем больше, тем хуже, другие измеряют количество пара, которое мембрана может пропустить сквозь себя за единицу времени.
Мне понятнее тесты, которые показывают производительность мембраны в граммах, на метр, в сутки. Но там тоже нюансы, «прямая чашка», «перевернутая чашка» — показатели могут отличаться в два раза.
Чаще мы имеем показатели пароприцаемости, выраженной в граммах, на метр квадратный, в сутки. Например, 15-20 000 гр/м2/24 ч. И здесь меня лично меньшие цифры не устраивают. Всякие мембраны типа 5Х5 – это фуфло и, даже 10Х10 — меня мало интересуют.
Например, 15-20 000 гр/м2/24 ч. И здесь меня лично меньшие цифры не устраивают. Всякие мембраны типа 5Х5 – это фуфло и, даже 10Х10 — меня мало интересуют.
Частое заблуждение, что мембрана -это такая чудесная штука, которая обеспечивает чудесную дышимость и, столь же чудесную, водонепроницаемость.
Нет. Резина держит больше любой мембраны, а марля дышит лучше.
Ну и отлично, далась нам эта дышимость! Но резиновые ботинки заполнятся потом, вода теплопроводнее воздуха раз в тридцать, вы замерзли.
Тогда, может и черт с ней, с водонепроницаемостью? Ботинки без мембраны дышат лучше, чем с ней. Но ботинки промокнут под дождем или в снегу, вода теплопроводнее воздуха — опять замерзли.
Без противогаза дышать лучше, чем в нем, но для чего-то он нужен…
Если завощить (покрыть воском) марлю, она станет более водонепроницаемой, но потеряет в дышимости, хотя способ древний, известный и логичный. Конечно, марля тут для абсурдности примера. Или, лучше, понаделать дырочек в резине, сапог станет лучше дышать, но вероятнее всего, промокнет.
Конечно, марля тут для абсурдности примера. Или, лучше, понаделать дырочек в резине, сапог станет лучше дышать, но вероятнее всего, промокнет.
Снаружи мембраны у нас: ветер, дождь, снег, под мембраной у нас испарения нашего тела, пот.
Если вам одновременно нужно препятствовать проникновению одного и удалению другого, простого решения не найти. Нужен такой материал, который не пропустит воду внутрь, но даст выйти испарению, поту.
В общем, мембрана – это всегда компромисс между водонепроницаемостью и дышимостью. Мембрана – не чудо, не колония наноботов, не УФМС и, даже, не ЖКХ по непущанию воды снаружи и по выводу пота изнутри. Это вопрос давления и температур. Точнее их разницы под мембраной и снаружи. В физике существует процедура продавливания газа через металл. То есть при нужном давлении, наверное, любой материал может стать мембраной.
Параметры внешнего субстрата нам известны, внутреннего – тоже.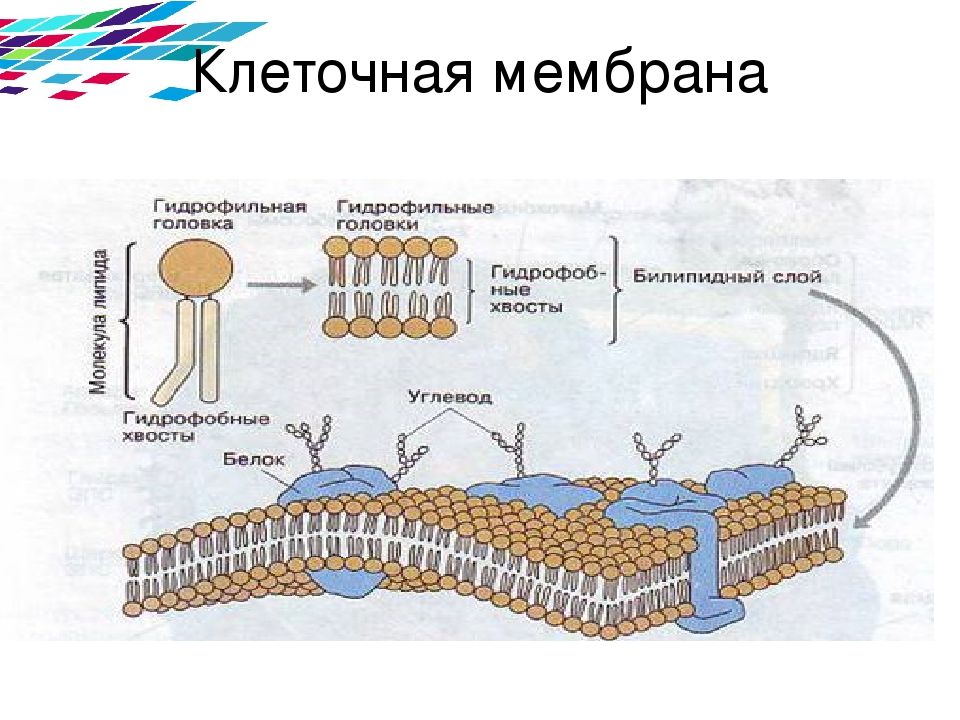 Температура наружных субстратов и внутренних, и, соответственно, их активность — разные. Одно из основных условий: снаружи мембраны должно быть холоднее, с внутренней стороны, соответственно, теплее. Появляется разница давлений обеспечивающая, так сказать, тягу — изнутри – наружу.
Температура наружных субстратов и внутренних, и, соответственно, их активность — разные. Одно из основных условий: снаружи мембраны должно быть холоднее, с внутренней стороны, соответственно, теплее. Появляется разница давлений обеспечивающая, так сказать, тягу — изнутри – наружу.
Остается найти такой материал для мембраны, чтобы в необходимом диапазоне температур минимально препятствовал бы тяге и был бы, при этом, максимально непроницаем для воды.
Чем и занимаются по сей день производители мембран. Практическим путем пришли к тому, что водонепроницаемость более 20 000 мм водяного столба, уже достаточна для большинства случаев.
Теперь — дышимость. С ней труднее. Как я уже говорил, показатели меньше 15-20 000 гр./м/24 ч – мне не интересны. Но опять вылезают нюансы. Показатели могут быть заоблачные, и 40 000 и 70 000 гр./м/24 ч, а вы при этом сухости внутри вдруг не ощущаете.
А все потому, что они, мембраны разные еще и по строению, и я об этом упоминал, помните: поровые, беспоровые, волоконные, гибридные.
Здесь практику нужно понять только одно, паропроницаемость поровых и волоконных мембран, обеспечивается порами. Т.е. микро, а то и наноотверстиями в теле мембраны, которые непроходимы для воды, но проходимы для более активной, нагретой массы ваших испарений. Можно назвать это — сухой тип.
Или же, оная паропроницаемость обеспечена молекулярной структурой беспоровой или же гибридной мембраны. В этом случае пару нужно, для начала, конденсироваться на внутренней поверхности мембраны и только потом разница давлений увлечет это все вовне. В этом случае мы будем ощущать некоторую увлажненность внутри. Это мы назовем — мокрый тип.
Но это все в идеале. В жизни все очень зависит от условий, в которых вы находитесь и от уровня вашей активности, то есть массы производимых испарений. Если снаружи будет слишком тепло, мембрана будет дышать хуже. Если будет слишком холодно, мембрана может замерзнуть, точнее замерзнут ваши испарения на выходе и так же снизят производительность мембраны, вплоть до полной остановки, если речь пойдет об арктических минусах при высокой влажности.
Современные беспоровые, гидрофильные мембраны имеют выдающиеся показатели дышимости, до 70 000 гр./м/24ч, но будут работать в более узком диапазоне температур.
Показатели поровых, поскромнее 16-32 000 гр./м/24ч, но работают в более широком диапазоне.
Мембранные ткани, это не мембрана, это ткани, вовсе не обязательно тканые, соединенные с мембраной. Показатели голой мембраны всегда отличаются от показателей ткани с мембраной. Это зависит от толщины слоя ткани верха, мембраны и толщины слоя подкладки. Эти слои защищают мембрану от повреждений. Чем они мощнее, тем прочнее изделие. Но сами понимаете, это не может не сказаться на способности мембраны «дышать». Цифры, которые я приводил, относятся к показателям ламинатов.
Когда говорят: трехслойная мембрана, это значит, что слой ткани верха, слой мембраны и слой ткани подкладки соединены/ламинированы так, что кажутся одним слоем. Это наиболее предпочтительный, с точки зрения аутдорной эксплуатации вариант. Изделие из такой ткани можно сунуть в воду, вынуть, встряхнуть от воды и, спокойно, надеть на себя.
Сегодня производители активно экспериментируют с материалом и структурой подкладочного слоя, и это изрядно сказывается на показателях мембранного ламината в целом.
Часто мы видим, что слой подкладки выполнен не в виде ламинированной ткани, а в виде напыления некоей пленки. Так называемый, двух с половиной-слойный ламинат. Это легче, компактней, дешевле, но менее прочно.
Еще бывает так, что подкладка представляет собой не соединенный с остальными двумя слоями, слой сетки – такую конструкцию называют двухслойной, поскольку соединены только два слоя: верх и мембрана. Этот вариант для аутдора не годится, поскольку, во-первых сетка при намокании будет долго сохнуть, во-вторых, в случае отрицательных температур между сеткой подкладки и мембраной будет накапливаться иней, и его будет много и удалить его, не разрушив сетку, станет нетривиальной задачей.
Из основных моментов осталось сказать только, что слой верха тоже влияет на работу ламината. Представляя собой некую толщину, и будучи пропитан водой, он будет препятствием для корректной работы мембраны, поэтому верх ламината пропитывают водоотталкивающими составами еще на фабрике. И не худо было бы проделывать эту процедуру в дальнейшем, по мере того, как вы будете замечать, что капли воды уже не скатываются с вашей куртки, а сразу образуют мокрое пятно.
И пару моментов напоследок:
— надо понимать, что мембрана под водой работать будет почти никак
— в условиях Северного полюса мембранные изделия почти бесполезны. Из-за высокой влажности и низких температур они будут быстро обмерзать с образованием наледи сперва снаружи изделия, затем внутри. Есть, конечно, лайфхак, надеть поверх мембраны тонкий флис, или какой другой легкий слой и обмерзать будет уже он, а мембрана начнет работать.
К слову, на Южном полюсе такой влажности нет, и там вовсю используют мембранные изделия.
Подытоживая: мембраны это не такая чудо штука, которую, если купил, то она будет неслышно дышать за вас так, что все будет сухо и комфортно. Как дома на диване. Но мембраны — это хорошо, а хорошие мембраны позволяют утащить с собой комфорт очень далеко, а плохие мембраны приносят лишь горечь разочарования и облегчение только в кошельке.
Александр Родичев. Трамонтана.
P.S. Стоит отметить, что Саша довольно категоричен в показаниях мембраны, и меньше, чем на 15000-20000 не согласен. Однако, если вам «по грибы» или переждать короткий кусочек непогоды, а не забивать крючья на стене, то 10000/10000 минимально и достаточно. Для примера, если вы наступили коленом в лужу — то создали давление около 8000 мм. Под лямками рюкзака создается примерно такое же давление (еще и длительное по времени) — это самое «тонкое» место в куртке.
5000/5000 и около того, действительно, нерабочая вещь — вы либо промокните снаружи, либо — изнутри. Проще купить проветриваемое пончо.
Ну и отдельно стоят разные легкоходные вещи. Если вы видите показатели 20000 на 20000 и с весом 200 грамм, то не ждите от нее долговечности и надежности. Берегите ее, не таскайте с рюкзаком по лесу.
И всегда советуйтесь с консультантами — плохого не посоветуют!
Мембранные куртки тут
Брюки тут
Топ-5 мембран на все случаи жизни
Несмотря на то, что в названии статьи сказано обо всех случаях жизни, конечно, надо понимать, что производители мембранных тканей – не джины из бутылки, и решить все проблемы пользователей не способны, хоть и очень стараются. Дабы составить представление о том, что такое мембранные ткани и какие задачи они способны решать, давайте коротко разберемся в строении мембран, способах производства и свойствах.
Виды мембран
Мембранные ткани различаются строением, методом производства и образом действия. По строению мембраны делятся на беспоровые, поровые, комбинированные и электроспиннинговые.
Беспоровые мембраны (гидрофильные) – сплошное покрытие, осуществляющее транспортировку влаги изнутри за счет диффузии. Необходима разница в давлении и влажности. Поэтому, прежде чем выйти наружу, влага скапливается внутри мембраны в достаточном для вытеснения на поверхность количестве. Материал всегда ощущается слегка влажным. Соответственно, беспоровая мембрана не слишком хорошо выводит пары влаги при открытой вентиляции, влажной погоде и при минусовых температурах. К положительным качествам можно отнести долговечность, высокие показатели водостойкости и паропроницаемости, абсолютную ветроустойчивость и относительно низкую стоимость. Наиболее известные примеры: Toray Dermizax, Marmot Membrane, Mountain Hardware Conduit.
Поровые мембраны (гидрофобные) – представляют собой тонкий слой полиуретана или тефлона (политетрафторэтилена – ПТФЭ), растянутый до такой степени, что распадается на отдельные волокна, между которыми образуются поры. Поровые мембраны хорошо работают на отведение паров влаги и имеют хорошую водостойкость. Такие мембраны работают во влажной атмосфере и при низких температурах. Однако, поры быстро загрязняются, а сама мембрана слишком нежна и подвержена повреждениям от механического воздействия. Наиболее известные примеры: Gore-Tex 30-летней давности, первые мембраны eVent и другие.
Поровая мембрана под микроскопом
Комбинированные мембранные материалы сочетают в себе поровую мембрану и беспоровое покрытие, защищающее ее от механических повреждений. Классический представитель данной конструкции – современный Gore-Tex. Беспоровое покрытие значительно тоньше стандартной беспоровой полиуретановой мембраны, а потому ее недостатки практически не проявляются. Таким образом, комбинированный мембранный материал обладает преимуществами поровых мембран и надежностью беспорового покрытия.
Электроспиннинговый мембранный материал — относительно свежее изобретение. Яркими представителями служат Polartec Neoshell (2012 год), Outdoor Research AscentShell (2016 год) и The North Face Futurelight™ (2019 год). Особенностью конструкции является нанопокрытие из полиуретана, наносимое практически на любую ткань с помощью множества миниатюрных сопел. Процесс схож с работой струйного принтера. Толщина полиуретановых нитей настолько мала, что на поверхности ткани образуется тончайшая пространственная решетка, обладающая свойствами мембраны. Плотность мембранной пленки очень низка, ткань сохраняет эластичность и имеет чрезвычайно высокие показатели паропроницаемости. Благодаря контролируемому процессу характеристиками такой мембраны можно управлять еще во время нанесения нановолокон на ткань. Считается, что данная технология – будущее outdoor индустрии.
Ради чего же проводятся все эти дорогостоящие исследования, запускаются невероятные технологические процессы, создаются производственные мощности и делаются сумасшедшие открытия? Ведь можно просто надеть полиэтиленовый пакет размером с человеческий организм и остаться сухим во время сильнейшего ливня. Да, если вы бежите из дачного домика накрыть огурцы в огороде, чтобы их не побило градом. Люди, покоряющие вершины гор и проходящие маршрут в суровых природных условиях, нуждаются в чем-то большем, чем полиэтиленовый пакет. Им необходима надежность, безопасность, максимально возможный комфорт и минимум мыслей о том, как работает их одежда, подведет ли она в самый ответственный момент. Им нужно ощущение сухости изнутри. Прочность и долговечность. Возможность довериться своему снаряжению, поскольку от этого часто зависит их жизнь.
Свойства мембран
Итак, что мы можем получить от мембранного материала?
Паропроницаемость – способность ткани выводить наружу избыточную влагу, которая непременно образуется у человека во время интенсивных нагрузок. Влага выводится в виде пара после испарения с поверхности кожи. Эта способность защищает от переохлаждения в холодную погоду и от перегрева во время физической активности.
Водостойкость – свойство мембраны препятствовать проникновению влаги снаружи. Пар и капля воды состоят из молекул одинакового размера, поскольку это всего лишь разные агрегатные состояния воды. Это мы знаем из школьного курса физики. Однако, связь между молекулами в капле значительно выше, капля плотнее, а значит, ее проще задержать на поверхности. Так и работает мембрана. Вода снаружи задерживается, не проникая внутрь, а избыточный пар изнутри свободно выводится на поверхность.
И тут кроется задачка, справиться с которой производителям мембранных материалов пока не под силу. Если придать мембране высокие показатели паропроницаемости, она потеряет в водостойкости. Сделав мембрану максимально водостойкой, чрезвычайно сложно придать ей высокие влагоотводящие показатели. Должен соблюдаться определенный баланс. Или теряется универсальность.
Ветроустойчивость или воздухопроницаемость – характеристика, описывающая возможность мембранной ткани пропускать воздух или противостоять ветру. Ветер может быть как помощником, охлаждающим организм во время высокой активности, так и ярым противником, выдувающим из-под одежды драгоценное тепло. Чем более устойчива к ветру мембранная ткань куртки или брюк, тем выше вероятность сохранения внутреннего микроклимата даже в экстремальных условиях. Показатели воздухопроницаемости крайне редко указываются производителями мембранных тканей. Чаще всего приблизительно пишут о процентах ветроустойчивости.
Топ-5
Рассмотрим пять наиболее известных мембранных тканей, достаточно универсальных, чтобы подойти «на все случаи жизни». Как мы уже поняли, всякая универсальность имеет границы. Поэтому выбирать мембранную ткань стоит, исходя из условий использования и собственных требований к конкретному снаряжению.
А вот и «случаи жизни» – сферы деятельности, в которых нам необходима высокотехнологичная одежда и обувь с мембраной:
- все виды альпинизма
- скалолазание на естественном рельефе
- зимние виды спорта: сноуборд, горные лыжи, в том числе экстремальные дисциплины, такие как фрирайд и хелиски.
- хайкинг, треккинг и горный туризм
- рыбалка и охота
- мотоспорт и автоспорт
Gore-Tex Pro
Согласно заявлению производителя – мембранная ткань из категории Ultimate. Бескомпромиссная защита от ветра и воды, высокие показатели паропроницаемости и отменная прочность. Везде, где от одежды требуется полная отдача, подойдет мембранная ткань Gore-Tex Pro.
Мембранные ткани Gore-Tex Pro имеют высокие показатели паропроницаемости, следовательно, при интенсивных нагрузках внутренний микроклимат будет сохраняться, что поможет избежать перегрева или переохлаждения в суровых условиях. К тому же образующийся во время двигательной активности липкий пот – явление малоприятное. Дождь, снег и попадание под водопад мембрана держит очень долгое время. В ботинках Gore-Tex Pro можно смело измерять глубину луж и долго идти по горным тропам в проливной дождь. Сухость изнутри гарантирована. Ледяной ветер остужает одежду-оболочку, но не проникает внутрь через ткань, а значит, не выдувает тепло и не охлаждает организм.
Показатели в числах:
- паропроницаемость – RET <6 м² Pa/W (тест, определяющий способность ткани сопротивляться проникновению пара; чем ниже показатель, тем лучше паропроницаемость)
- водостойкость – 28 000 мм водяного столба
Конструкция Gore-Tex Pro представляет собой 3 полноценных слоя: верхняя ткань, мембрана и внутренняя ткань. Внешний слой обычно имеет водоотталкивающую пропитку DWR, которая не позволяет ему намокать и накапливать влагу. Сухой внешний слой обеспечивает защиту от механических повреждений и беспрепятственную работу мембраны по транспортировке избыточной влаги от тела. Внутренний слой защищает мембрану от трения о средние и базовые слои одежды, не препятствует отводу влаги.
Мембрана Gore—Tex под микроскопом
Плюсы очевидны. Сюрпризы природы в виде дождя, снега и ветра обладателю комплекта одежды с мембраной Gore-Tex Pro не страшны. А значит, можно заниматься любимым видом деятельности, не отвлекаясь на мелочи. Однако если вам нравится, например, бег по пересеченной местности, и вы совершаете пробежки в любую погоду, включая июльскую жару, стоит обратить внимание на другие продукты Gore-Tex, более подходящие для теплой погоды.
Мембранные материалы Gore-Tex используют практически все известные производители снаряжения для экстремальных видов спорта. В нашем магазине это бренды Arcteryx, Asolo, Berghaus, Dakine, Haglofs, La Sportiva, Montura, Norrona, Mammut, Mountain Equipment, Mountain Hardwear, Patagonia и другие.
.
Toray Dermizax NX
Мембранная ткань Dermizax NX японского производителя Toray представляет последнее поколение беспоровых мембран. Очень тонкая и эластичная полиуретановая ткань, имеющая кристаллическую структуру, высочайшие показатели паропроницаемости и водостойкости. Поскольку такая ткань не имеет пор, она способна растягиваться до 200%. Прочная и устойчивая к жесткой эксплуатации, не забивается частицами грязи или кожного жира, совершенно не пропускает ветер. С использованием мембраны Dermizax NX производятся эффективно работающие трехслойные ткани для одежды outdoor.
Показатели в числах:
- паропроницаемость – 30 000 до 40 000 г/м²/24ч
- водостойкость – 20 000 мм водяного столба и выше
Транспортировка влаги на поверхность материала достигается за счет процесса диффузии, благодаря разнице во влажности изнутри и снаружи. Dermizax NX осуществляет перенос быстро, демонстрируя минимальный уровень конденсации, а время является важным показателем качества мембраны. Соответственно, при высоких температурах влага будет накапливаться быстрее, транспортировка тоже ускорится.
Структура мембраны Dermizax
Группа тканей Toray Dermizax напрямую соперничает с Gore-Tex по своим характеристикам и показателям.
Бренд с мембранами группы Dermizax, представленный в нашем магазине: Bergans.
.
The North Face Futurelight™
Фирменный мембранный материал от бренда The North Face, полученный посредством электроспиннинговой технологии. В компании назвали процесс производства «наноспиннинг».
Futurelight™ – трехслойная ткань. На внешний слой из переработанных материалов нанесена тончайшая полимерная сетка. Вместо пор – микроскопические промежутки между волокнами полиуретана. Внутренний слой – мягкая подкладка, также сделанная из переработанных материалов. Внешний слой ткани обрабатывается стойкой водоотталкивающей пропиткой DWR без полифторированных соединений в составе (PFC-Free).
По утверждению производителя наноструктура мембраны Futurelight™ позволяет существенно повысить показатели паропроницаемости без ущерба водонепроницаемости и долговечности, а процесс производства – задать эти свойства на этапе нанесения волокон полиуретана на ткань. В итоге получилась водостойкая, ветрозащитная, отлично «дышащая», тонкая, эластичная и прочная ткань, способная защитить пользователя в самых суровых условиях. Плотность мембранного слоя невысока и содержит до 85% воздуха, поэтому материал имеет малый вес, сохраняет некоторую воздухопроницаемость. Плюс, с помощью данной технологии можно создавать бесшовные переходы между более водостойкими и воздухопроницаемыми зонами на одежде. То есть, в стратегически расположенных зонах мембрана будет или защищать от проникновения воды извне, или помогать телу дышать, осуществляя транспортировку влаги на поверхность с большей эффективностью.
Несмотря на свежесть разработки, уже были проведены полевые и лабораторные испытания. Компания The North Face сотрудничает с американской организацией Underwriters Laboratories Inc. (далее – UL), занимающейся стандартизацией и сертификацией в области техники безопасности. UL подвергла ткань Futurelight™ тем же испытаниям на водостойкость, что использовались для пожарного снаряжения. На одежду сбрасывалось более 200 галлонов (757 л) воды в час. Futurelight™ выдержала испытание и получила сертификат UL, гарантирующий 100% водонепроницаемость при сохранении высокого уровня воздухопроницаемости. Однако, конкретные числа компанией не раскрываются.
Показатели паропроницаемости известны и являются максимальными из существующих на рынке – верхний возможный предел 75 000 г/м²/24 ч. Мембрана превосходно работает на выведение влаги и не позволяет конденсату образовываться на внутренней поверхности одежды.
Полевые испытания прошли успешно в экстремальных условиях гор от Эвереста до первого спуска на лыжах с вершины Лходзе.
В нашем магазине товары бренда с мембраной Futurelight™ можно посмотреть здесь: The North Face.
.
Patagonia h3No
h3No – собственная разработка компании Patagonia. История и идеология бренда базируются на гуманном отношении к природе, поэтому основной отличительной особенностью тканей Patagonia является включение в их состав переработанных и биоразлагаемых материалов. Трехслойная мембранная ткань h3No, детали производства которой не разглашаются, состоит из 100% переработанного нейлона, поликарбонатной мембраны с 13% биоразлагаемых компонентов и трикотажной подкладки. Плюс, стойкая водоотталкивающая пропитка без PFC – Deluge® DWR, которая считается более надежной, чем классическая DWR.
Чтобы продукция бренда служила дольше и менялась пользователями реже, материалам придана исключительная долговечность, прочность и износоустойчивость. Patagonia подвергает свои ткани жесточайшим тестам. Тест на прочность, например, называется «Killer Wash» – «стирка-убийца». Тест за 24 часа имитирует годы интенсивной эксплуатации во влажных условиях, проверяя продукцию на стойкость к заломам и истиранию. Тест на водостойкость предполагает три дня испытаний небольшим дождем, ливнями и на специальном оборудовании. Паропроницаемость тестируется по стандартам MVTR (Moisture Vapor Transmission Rate).
Показатели в числах:
- паропроницаемость: 15 000 г/м²/24ч
- водостойкость – 20000 мм водяного столба до теста Killer Wash и 10000 мм после теста
Таким образом, компания Patagonia вот уже несколько лет предлагает нашему вниманию одежду с собственной мембраной. Одежду, способную выдержать экстремальные нагрузки, полностью защитить от воды и ветра, эффективно транспортировать пары пота изнутри, препятствовать конденсации влаги и быстро сохнуть.
Одежда бренда Patagonia есть в наших магазинах.
.
Event DValpine
Мембранная ткань бренда Event производится компанией BHA Technologies с 1999 года. Огромный шаг вперед был сделан, когда появилась собственная технология Direct Venting™ (DV). Классическая поровая мембрана без покрытия быстро теряет свои свойства из-за загрязнения пор. Основными загрязнителями являются жиры, которые накапливаются в материале ePTFE (ПФТЭ) поскольку он олеофилен. Direct Venting™ Technology создало мембрану, которая всегда имеет открытые поры и не накапливает загрязнения. С этой целью на волокна мембраны наносится олеофобное покрытие, предотвращающее оседание жиров и масел и сохраняющее свойства ткани.
Благодаря технологии Direct Venting™ пары влаги свободно выходят через поры на поверхность. Материал не накапливает влагу, не нуждается в разнице давления для ее транспортировки, хорошо работает при низких температурах и в условиях высокой влажности. То есть, не имеет «болячек» первых беспоровых мембран. Организм человека даже при интенсивной нагрузке находится в так называемой «сухой зоне». Он достаточно охлаждается, чтобы не перегреться в результате неэффективного испарения, и не замерзает, поскольку влага не скапливается под одеждой.
Ламинат DValpine состоит из 3 слоев: верхний слой с обработкой DWR, мембрана с технологией Direct Venting™ и мягкая, комфортная подкладка, не препятствующая переносу влаги.
Показатели в числах:
- паропроницаемость: 20 000 г/м²/24ч
- водостойкость: 20000 мм водяного столба
В нашем магазине мембраны Event представлены брендом Hoka.
Бонус – Hydroshell Elite Pro
Hydroshell – мембранные ткани британской компании Berghaus, которая имеет пятидесятилетний опыт создания водонепроницаемого снаряжения. Впервые одежда с мембраной Hydroshell была представлена в 2015 году.
Hydroshell Elite Pro абсолютно водонепроницаема, обладает высокими показателями паропроницаемости, отличным соотношением прочности и веса. Сверхлегкая конструкция из 2.5 слоев, верхний из которых – прочный нейлон. Стойкая и долговечная водоотталкивающая обработка DWR, которую используют в Berghaus, не содержит полифторированных соединений в составе (PFC-Free). Производитель утверждает, что пропитка держится дольше своих аналогов и реже требует восстановления.
Показатели в числах:
- паропроницаемость: 20000 г/м2/24ч
- водостойкость: 20000 мм
В нашем магазине есть продукция бренда Berghaus с мембранами Hydroshell.
.
Заключение
Выбирать мембрану стоит, исходя из предполагаемого вида деятельности и его особенностей. Рассмотренные нами примеры максимально универсальны и способны защитить от суровых погодных условий.
Однако надо быть готовым к нескольким моментам, которые сложно обойти в процессе использования одежды из мембранных материалов.
- Куртка с мембраной не будет корректно выполнять свою задачу, если под ней обычные вещи, не поддерживающие систему слоев. Мембрана не сможет вывести влагу, если ее накапливает белье или свитер. Куртка будет работать в качестве дождевика, а внутри все равно образуется конденсат.
- У каждой мембраны есть предел времени или количества влаги, по окончании которого она начнет промокать. Это не значит, что материал плох. Просто он достиг своего предела.
- Мембрана с показателем водонепроницаемости 10 000 мм водяного столба защитит вас от сильного дождя, если вы не гуляете под ним весь день. Большинству пользователей такой степени защиты достаточно. От 20 000 мм и выше – рассчитаны на экстремальный уровень. Поэтому не гоняйтесь за цифрами, выбирайте по потребностям.
- Как и любые ткани, мембранные материалы постепенно изнашиваются и теряют свои свойства. Но можно продлить срок службы, если правильно ухаживать за своими вещами. О бережном отношении не говорим, ведь предназначены они для эксплуатации в экстремальных условиях. Хотя, это тоже помогло бы.
- Кроме Gore-Tex, Dermizax, Futurelight, h3No, Event и Hydroshell, существует огромное количество похожих по принципу действия мембранных материалов. Старайтесь не выбирать «noname» за цену и доступность. Процесс производства, тестирования и сертификации очень дорог. Мембрана не может быть дешевой. Такая покупка не решит проблему и не прослужит долго.
До встречи в горах!
Перевод выполнила Драгунова Анна
Cell Membranes — The Cell
Структура и функция клеток в значительной степени зависят от мембран, которые не только отделяют внутреннюю часть клетки от окружающей среды, но также определяют внутренние компартменты эукариотических клеток, включая ядро и цитоплазматические органеллы. Формирование биологических мембран основано на свойствах липидов, и все клеточные мембраны имеют общую структурную организацию: бислои фосфолипидов с ассоциированными белками. Эти мембранные белки отвечают за многие специализированные функции; некоторые действуют как рецепторы, которые позволяют клетке реагировать на внешние сигналы, некоторые отвечают за избирательный транспорт молекул через мембрану, а другие участвуют в переносе электронов и окислительном фосфорилировании.Кроме того, мембранные белки контролируют взаимодействия между клетками многоклеточных организмов. Общая структурная организация мембран, таким образом, лежит в основе множества биологических процессов и специализированных мембранных функций, которые будут подробно обсуждаться в следующих главах.
Мембранные липиды
Основными строительными блоками всех клеточных мембран являются фосфолипиды, которые представляют собой амфипатические молекулы, состоящие из двух гидрофобных цепей жирных кислот, связанных с фосфатсодержащей гидрофильной головной группой (см.).Поскольку их хвосты жирных кислот плохо растворимы в воде, фосфолипиды спонтанно образуют бислои в водных растворах, причем гидрофобные хвосты находятся внутри мембраны, а группы полярных головок открыты с обеих сторон, контактируя с водой (). Такие бислои фосфолипидов образуют устойчивый барьер между двумя водными отсеками и представляют собой основную структуру всех биологических мембран.
Рисунок 2.45
Фосфолипидный бислой. Фосфолипиды спонтанно образуют стабильные бислои, при этом их полярные головные группы подвергаются воздействию воды, а их гидрофобные хвосты находятся внутри мембраны.
Липиды составляют примерно 50% массы большинства клеточных мембран, хотя эта пропорция варьируется в зависимости от типа мембраны. Например, плазматические мембраны состоят примерно на 50% из липидов и 50% из белков. С другой стороны, внутренняя мембрана митохондрий содержит необычно высокую фракцию (около 75%) белка, что отражает обилие белковых комплексов, участвующих в переносе электронов и окислительном фосфорилировании. Липидный состав различных клеточных мембран также различается ().Плазматическая мембрана E. coli состоит преимущественно из фосфатидилэтаноламина, который составляет 80% от общего количества липидов. Плазматические мембраны млекопитающих более сложны и содержат четыре основных фосфолипида — фосфатидилхолин, фосфатидилсерин, фосфатидилэтаноламин и сфингомиелин, которые вместе составляют от 50 до 60% от общего количества липидов мембран. Помимо фосфолипидов, плазматические мембраны клеток животных содержат гликолипиды и холестерин, которые обычно составляют около 40% от общего количества молекул липидов.
Таблица 2.3
Липидный состав клеточных мембран a .
Важным свойством липидных бислоев является то, что они ведут себя как двумерные жидкости, в которых отдельные молекулы (как липиды, так и белки) могут свободно вращаться и двигаться в боковых направлениях (). Такая текучесть является важным свойством мембран и определяется как температурой, так и липидным составом. Например, взаимодействия между более короткими цепями жирных кислот слабее, чем между более длинными цепями, поэтому мембраны, содержащие более короткие цепи жирных кислот, менее жесткие и остаются жидкими при более низких температурах.Липиды, содержащие ненасыщенные жирные кислоты, аналогичным образом увеличивают текучесть мембран, поскольку наличие двойных связей вносит перегибы в цепочки жирных кислот, что затрудняет их объединение.
Рисунок 2.46
Подвижность фосфолипидов в мембране. Отдельные фосфолипиды могут вращаться и двигаться в боковом направлении внутри бислоя.
Благодаря своей структуре углеводородного кольца (см.), Холестерин играет особую роль в определении текучести мембран. Молекулы холестерина вставляются в бислой с их полярными гидроксильными группами, близкими к гидрофильным головным группам фосфолипидов ().Таким образом, жесткие углеводородные кольца холестерина взаимодействуют с участками цепей жирных кислот, которые примыкают к головным фосфолипидным группам. Это взаимодействие снижает подвижность внешних частей цепей жирных кислот, делая эту часть мембраны более жесткой. С другой стороны, введение холестерина препятствует взаимодействиям между цепями жирных кислот, тем самым поддерживая текучесть мембран при более низких температурах.
Рисунок 2.47
Введение холестерина в мембрану.Холестерин внедряется в мембрану со своей полярной гидроксильной группой, близкой к полярным головным группам фосфолипидов.
Мембранные белки
Белки являются другим основным компонентом клеточных мембран, составляя от 25 до 75% массы различных мембран клетки. Текущая модель мембранной структуры, предложенная Джонатаном Сингером и Гартом Николсоном в 1972 году, рассматривает мембраны как жидкую мозаику , в которой белки вставлены в липидный бислой (). В то время как фосфолипиды обеспечивают основную структурную организацию мембран, мембранные белки выполняют определенные функции различных мембран клетки.Эти белки делятся на два общих класса в зависимости от характера их ассоциации с мембраной. Интегральные мембранные белки встроены непосредственно в липидный бислой. Белки периферической мембраны не встраиваются в липидный бислой, но связаны с мембраной косвенно, обычно посредством взаимодействий с интегральными мембранными белками.
Рисунок 2.48
Жидкая мозаичная модель мембранной структуры. Биологические мембраны состоят из белков, встроенных в липидный бислой.Интегральные мембранные белки встраиваются в мембрану, обычно через α-спиральные области из 20-25 гидрофобных аминокислот. Некоторые (подробнее …)
Многие интегральные мембранные белки (называемые трансмембранными белками) охватывают липидный бислой, причем части, обнаженные с обеих сторон мембраны. Перекрывающие мембрану части этих белков обычно представляют собой α-спиральные области из 20-25 неполярных аминокислот. Гидрофобные боковые цепи этих аминокислот взаимодействуют с цепями жирных кислот мембранных липидов, и образование α-спирали нейтрализует полярный характер пептидных связей, как обсуждалось ранее в этой главе в отношении сворачивания белков.Как и фосфолипиды, трансмембранные белки представляют собой амфипатические молекулы, гидрофильные части которых подвергаются воздействию водной среды с обеих сторон мембраны. Некоторые трансмембранные белки покрывают мембрану только один раз; другие имеют несколько участков, перекрывающих мембрану. Большинство трансмембранных белков плазматических мембран эукариот были модифицированы путем добавления углеводов, которые экспонируются на поверхности клетки и могут участвовать во взаимодействиях между клетками.
Белки также могут быть закреплены в мембранах липидами, которые ковалентно присоединены к полипептидной цепи (см. Главу 7).Определенные липидные модификации прикрепляют белки к цитозольным и внеклеточным поверхностям плазматической мембраны. Белки могут быть прикреплены к цитозольной стороне мембраны либо путем добавления 14-углеродной жирной кислоты (миристиновой кислоты) к их аминоконцу, либо путем добавления либо 16-углеродной жирной кислоты (пальмитиновая кислота), либо 15- или 20-углеродные пренильные группы к боковым цепям остатков цистеина. Альтернативно, белки прикрепляются к внеклеточной поверхности плазматической мембраны путем добавления гликолипидов к их карбоксиконцу.
Транспорт через клеточные мембраны
Избирательная проницаемость биологических мембран для малых молекул позволяет клетке контролировать и поддерживать свой внутренний состав. Только небольшие незаряженные молекулы могут свободно диффундировать через бислои фосфолипидов (). Небольшие неполярные молекулы, такие как O 2 и CO 2 , растворимы в липидном бислое и поэтому могут легко проникать через клеточные мембраны. Небольшие незаряженные полярные молекулы, такие как H 2 O, также могут диффундировать через мембраны, но более крупные незаряженные полярные молекулы, такие как глюкоза, не могут.Заряженные молекулы, такие как ионы, не могут диффундировать через бислой фосфолипидов независимо от размера; даже ионы H + не могут пересекать липидный бислой путем свободной диффузии.
Рисунок 2.49
Проницаемость фосфолипидных бислоев. Небольшие незаряженные молекулы могут свободно диффундировать через бислой фосфолипидов. Однако бислой непроницаем для более крупных полярных молекул (таких как глюкоза и аминокислоты) и для ионов.
Хотя ионы и большинство полярных молекул не могут диффундировать через липидный бислой, многие такие молекулы (например, глюкоза) способны пересекать клеточные мембраны.Эти молекулы проходят через мембраны под действием определенных трансмембранных белков, которые действуют как переносчики. Такие транспортные белки определяют избирательную проницаемость клеточных мембран и, таким образом, играют критическую роль в функции мембран. Они содержат несколько участков, охватывающих мембрану, которые образуют проход через липидный бислой, позволяя полярным или заряженным молекулам пересекать мембрану через поры белка, не взаимодействуя с цепями гидрофобных жирных кислот мембранных фосфолипидов.
Как подробно обсуждалось в главе 12, существует два общих класса мембранных транспортных белков (). Канальные белки образуют открытые поры через мембрану, позволяя свободно проходить любой молекуле подходящего размера. Ионные каналы, например, позволяют проходить через плазматическую мембрану неорганическим ионам, таким как Na + , K + , Ca 2+ и Cl —. Будучи открытыми, белки каналов образуют небольшие поры, через которые ионы соответствующего размера и заряда могут пересекать мембрану путем свободной диффузии.Поры, образованные этими белками каналов, не открыты постоянно; скорее, они могут выборочно открываться и закрываться в ответ на внеклеточные сигналы, позволяя клетке контролировать движение ионов через мембрану. Такие регулируемые ионные каналы особенно хорошо изучены в нервных и мышечных клетках, где они опосредуют передачу электрохимических сигналов.
Рисунок 2.50
Канал и белки-носители. (A) Канальные белки образуют открытые поры, через которые молекулы подходящего размера (например,г., ионы) могут пересекать мембрану. (B) Белки-носители избирательно связывают небольшую молекулу, которую необходимо транспортировать, а затем претерпевают конформацию (подробнее …)
В отличие от канальных белков, белки-носители избирательно связываются и транспортируют определенные небольшие молекулы, такие как глюкоза. Вместо того, чтобы формировать открытые каналы, белки-носители действуют как ферменты, облегчая прохождение определенных молекул через мембраны. В частности, белки-носители связывают определенные молекулы и затем претерпевают конформационные изменения, которые открывают каналы, по которым молекула, которая должна транспортироваться, может проходить через мембрану и высвобождаться с другой стороны.
Как описано выше, молекулы, транспортируемые каналом или белками-носителями, пересекают мембраны в энергетически выгодном направлении, определяемом концентрацией и электрохимическими градиентами — процесс, известный как пассивный транспорт. Однако белки-носители также обеспечивают механизм, посредством которого изменения энергии, связанные с транспортировкой молекул через мембрану, могут быть связаны с использованием или производством других форм метаболической энергии, так же, как ферментативные реакции могут быть связаны с гидролизом или синтезом АТФ.Например, молекулы могут транспортироваться через мембрану в энергетически неблагоприятном направлении (например, против градиента концентрации), если их транспорт в этом направлении связан с гидролизом АТФ в качестве источника энергии — процесс, называемый активным транспортом (). Таким образом, свободная энергия, запасенная в виде АТФ, может использоваться для управления внутренним составом клетки, а также для управления биосинтезом составляющих клетки.
Рисунок 2.51
Модель активного транспорта. Модель активного переноса Энергия, полученная в результате гидролиза АТФ, используется для переноса H + против электрохимического градиента (от низкой до высокой концентрации H + ).Связывание H + сопровождается фосфорилированием носителя (подробнее …)
.
Клеточные мембраныи жидкая мозаика, модель
Компоненты плазменных мембран
Плазматическая мембрана защищает клетку от внешней среды, опосредует клеточный транспорт и передает клеточные сигналы.
Цели обучения
Опишите функцию и компоненты плазматической мембраны
Основные выводы
Ключевые моменты
- Основными компонентами плазматической мембраны являются липиды (фосфолипиды и холестерин), белки и углеводы.
- Плазматическая мембрана защищает внутриклеточные компоненты от внеклеточной среды.
- Плазматическая мембрана опосредует клеточные процессы, регулируя материалы, входящие и выходящие из клетки.
- Плазматическая мембрана несет маркеры, которые позволяют клеткам узнавать друг друга и могут передавать сигналы другим клеткам через рецепторы.
Ключевые термины
- плазматическая мембрана : полупроницаемый барьер, окружающий цитоплазму клетки.
- рецептор : белок на клеточной стенке, который связывается с определенными молекулами, чтобы они могли всасываться в клетку.
Структура плазменных мембран
Плазматическая мембрана (также известная как клеточная мембрана или цитоплазматическая мембрана) — это биологическая мембрана, которая отделяет внутреннюю часть клетки от внешней среды.
Основная функция плазматической мембраны — защищать клетку от окружающей среды. Состоящая из фосфолипидного бислоя со встроенными белками, плазматическая мембрана избирательно проницаема для ионов и органических молекул и регулирует перемещение веществ в клетки и из них.Плазменные мембраны должны быть очень гибкими, чтобы определенные клетки, такие как красные и белые кровяные тельца, могли изменять форму при прохождении через узкие капилляры.
Плазматическая мембрана также играет роль в закреплении цитоскелета, чтобы придать форму клетке, и в прикреплении к внеклеточному матриксу и другим клеткам, помогая группировать клетки вместе для образования тканей. Мембрана также поддерживает клеточный потенциал.
Короче говоря, если ячейка представлена замком, плазматическая мембрана — это стена, которая обеспечивает структуру для зданий внутри стены, регулирует, какие люди покидают и входят в замок, и передает сообщения в соседние замки и из них.Подобно тому, как дыра в стене может стать катастрофой для замка, разрыв плазматической мембраны заставляет клетку лизироваться и погибать.
Плазматическая мембрана : Плазматическая мембрана состоит из фосфолипидов и белков, которые создают барьер между внешней средой и клеткой, регулируют транспортировку молекул через мембрану и связываются с другими клетками через белковые рецепторы.
Плазменная мембрана и клеточный транспорт
Движение вещества через избирательно проницаемую плазматическую мембрану может быть «пассивным» —i.е., происходящий без ввода клеточной энергии — или «активный», то есть его транспортировка требует от клетки расходовать энергию.
Клетка задействует ряд транспортных механизмов, в которых задействованы биологические мембраны:
- Пассивный осмос и диффузия: переносит газы (например, O 2 и CO 2) и другие небольшие молекулы и ионы
- Трансмембранные белковые каналы и переносчики: транспортирует небольшие органические молекулы, такие как сахара или аминокислоты
- Эндоцитоз: переносит большие молекулы (или даже целые клетки), поглощая их
- Экзоцитоз: удаляет или выделяет такие вещества, как гормоны или ферменты
Плазменная мембрана и клеточная сигнализация
Одной из наиболее сложных функций плазматической мембраны является ее способность передавать сигналы через сложные белки.Эти белки могут быть рецепторами, которые работают как приемники внеклеточных входов и как активаторы внутриклеточных процессов, или маркерами, которые позволяют клеткам узнавать друг друга.
Мембранные рецепторы обеспечивают сайты внеклеточного прикрепления для эффекторов, таких как гормоны и факторы роста, которые затем запускают внутриклеточные ответы. Некоторые вирусы, такие как вирус иммунодефицита человека (ВИЧ), могут захватывать эти рецепторы, чтобы проникнуть в клетки, вызывая инфекции.
Мембранные маркеры позволяют клеткам узнавать друг друга, что жизненно важно для клеточных сигнальных процессов, влияющих на формирование тканей и органов на раннем этапе развития.Эта функция маркирования также играет более позднюю роль в различении иммунного ответа «я» — «не-я». Белки-маркеры на эритроцитах человека, например, определяют группу крови (A, B, AB или O).
Жидкая мозаика Модель
Модель жидкой мозаики описывает структуру плазматической мембраны как мозаику из фосфолипидов, холестерина, белков и углеводов.
Цели обучения
Описание жидкой мозаичной модели клеточных мембран
Основные выводы
Ключевые моменты
- Основная ткань мембраны состоит из амфифильных или двойных молекул фосфолипидов.
- Интегральные белки, второй главный компонент плазматических мембран, полностью интегрированы в структуру мембраны, их гидрофобные области, охватывающие мембрану, взаимодействуют с гидрофобной областью фосфолипидного бислоя.
- Углеводы, третий основной компонент плазматических мембран, всегда находятся на внешней поверхности клеток, где они связаны либо с белками (образующими гликопротеины), либо с липидами (образующими гликолипиды).
Ключевые термины
- амфифильный : имеющий одну поверхность, состоящую из гидрофильных аминокислот, и противоположную поверхность, состоящую из гидрофобных (или липофильных) аминокислот.
- гидрофильный : обладает сродством к воде; способен впитывать или намокать водой, «водолюбив».
- гидрофобный : не обладает сродством к воде; не может впитывать или намокать водой, «боязнь воды».
Модель жидкой мозаики была впервые предложена С.Дж. Сингер и Гарт Л. Николсон в 1972 году объяснили структуру плазматической мембраны. Модель со временем несколько эволюционировала, но она по-прежнему лучше всего объясняет структуру и функции плазматической мембраны в том виде, в котором мы их теперь понимаем.Модель жидкой мозаики описывает структуру плазматической мембраны как мозаику компонентов, включая фосфолипиды, холестерин, белки и углеводы, что придает мембране жидкий характер. Плазменные мембраны имеют толщину от 5 до 10 нм. Для сравнения, красные кровяные тельца человека, видимые с помощью световой микроскопии, имеют ширину примерно 8 мкм, или примерно в 1000 раз шире плазматической мембраны. Соотношение белков, липидов и углеводов в плазматической мембране зависит от типа клетки.Например, миелин содержит 18% белка и 76% липидов. Внутренняя мембрана митохондрий содержит 76% белка и 24% липидов.
| Компоненты плазменной мембраны | |
|---|---|
| Компонент | Расположение |
| Фосфолипид | Основная ткань мембраны |
| Холестерин | Присоединяется между фосфолипидами и между двумя слоями фосфолипидов |
| Интегральные белки (например, интегрины) | Встраивается в фосфолипидный слой (слои).Может или не может проникать через оба слоя. |
| Периферические белки | На внутренней или внешней поверхности бислоя фосфолипидов; не встраивается в фосфолипиды |
| Углеводы (компоненты гликопротеинов и гликолипидов) | Обычно прикрепляется снаружи мембранного слоя |
Основными компонентами плазматической мембраны являются липиды (фосфолипиды и холестерин), белки и углеводы, связанные с некоторыми липидами и некоторыми белками.
Жидкая мозаичная модель плазматической мембраны : Жидкая мозаичная модель плазматической мембраны описывает плазматическую мембрану как жидкую комбинацию фосфолипидов, холестерина и белков. Углеводы, прикрепленные к липидам (гликолипидам) и белкам (гликопротеинам), выходят из обращенной наружу поверхности мембраны.
Основная ткань мембраны состоит из амфифильных или двойно-любящих молекул фосфолипидов. Гидрофильные или водолюбивые области этих молекул контактируют с водной жидкостью как внутри, так и снаружи клетки.Гидрофобные или ненавидящие воду молекулы обычно неполярны. Молекула фосфолипида состоит из трехуглеродного глицеринового остова с двумя молекулами жирных кислот, присоединенными к атомам углерода 1 и 2, и фосфатсодержащей группой, присоединенной к третьему атому углерода. Такое расположение дает всей молекуле область, описываемую как ее голова (фосфатсодержащая группа), которая имеет полярный характер или отрицательный заряд, и область, называемую хвостом (жирные кислоты), которая не имеет заряда. Они взаимодействуют с другими неполярными молекулами в химических реакциях, но обычно не взаимодействуют с полярными молекулами.При помещении в воду гидрофобные молекулы имеют тенденцию образовывать шар или кластер. Гидрофильные области фосфолипидов имеют тенденцию образовывать водородные связи с водой и другими полярными молекулами как снаружи, так и внутри клетки. Таким образом, поверхности мембраны, обращенные внутрь и снаружи клетки, являются гидрофильными. Напротив, середина клеточной мембраны гидрофобна и не взаимодействует с водой. Следовательно, фосфолипиды образуют превосходную двухслойную липидную клеточную мембрану, которая отделяет жидкость внутри клетки от жидкости вне клетки.
Агрегация фосфолипидов : В водном растворе фосфолипиды имеют тенденцию располагаться так, чтобы их полярные головки были обращены наружу, а их гидрофобные хвосты были обращены внутрь.
Структура молекулы фосфолипида : Эта молекула фосфолипида состоит из гидрофильной головки и двух гидрофобных хвостов. Гидрофильная головная группа состоит из фосфатсодержащей группы, присоединенной к молекуле глицерина. Гидрофобные хвосты, каждый из которых содержит насыщенную или ненасыщенную жирную кислоту, представляют собой длинные углеводородные цепи.
Белки составляют второй основной компонент плазматических мембран. Интегральные белки (некоторые специализированные типы называются интегринами), как следует из их названия, полностью интегрированы в структуру мембраны, и их гидрофобные области, охватывающие мембрану, взаимодействуют с гидрофобной областью фосфолипидного бислоя. Однопроходные интегральные мембранные белки обычно имеют гидрофобный трансмембранный сегмент, состоящий из 20-25 аминокислот. Некоторые охватывают только часть мембраны, соединяясь с одним слоем, в то время как другие простираются от одной стороны мембраны к другой и открываются с обеих сторон.Некоторые сложные белки состоят из до 12 сегментов одного белка, которые сильно свернуты и встроены в мембрану. Этот тип белка имеет гидрофильную область или области и одну или несколько умеренно гидрофобных областей. Такое расположение областей белка имеет тенденцию ориентировать белок рядом с фосфолипидами, при этом гидрофобная область белка примыкает к хвостам фосфолипидов, а гидрофильная область или области белка выступают из мембраны и контактируют с цитозолем или внеклеточной жидкости.
Структура интегральных мембранных белков : Интегральные мембранные белки могут иметь одну или несколько альфа-спиралей, охватывающих мембрану (примеры 1 и 2), или они могут иметь бета-листы, которые охватывают мембрану (пример 3).
Углеводы — третий важный компонент плазматических мембран. Они всегда находятся на внешней поверхности клеток и связаны либо с белками (образуя гликопротеины), либо с липидами (образуя гликолипиды). Эти углеводные цепи могут состоять из 2-60 моносахаридных единиц и могут быть как прямыми, так и разветвленными.Наряду с периферическими белками углеводы образуют на поверхности клетки специализированные участки, которые позволяют клеткам узнавать друг друга. Эта функция распознавания очень важна для клеток, поскольку позволяет иммунной системе различать клетки тела (называемые «самими») и чужеродные клетки или ткани (так называемые «чужие»). Подобные типы гликопротеинов и гликолипидов находятся на поверхности вирусов и могут часто меняться, не позволяя иммунным клеткам распознавать их и атаковать их. Эти углеводы на внешней поверхности клетки — углеводные компоненты как гликопротеинов, так и гликолипидов — вместе называются гликокаликсом (что означает «сахарное покрытие»).Гликокаликс обладает высокой гидрофильностью и привлекает большое количество воды к поверхности клетки. Это помогает во взаимодействии клетки с ее водной средой и в способности клетки получать вещества, растворенные в воде.
Текучесть мембраны
Мозаичный характер мембраны, ее фосфолипидный химический состав и присутствие холестерина способствуют текучести мембраны.
Цели обучения
Объясните функцию текучести мембран в структуре клеток
Основные выводы
Ключевые моменты
- Мембрана жидкая, но также довольно жесткая и может лопнуть при проникновении внутрь или при попадании в клетку слишком большого количества воды.
- Мозаичный характер плазматической мембраны позволяет очень тонкой игле легко проникать в нее, не вызывая ее разрыва, и позволяет ей самоуплотняться при извлечении иглы.
- Если насыщенные жирные кислоты сжимаются при понижении температуры, они давят друг на друга, образуя плотную и довольно жесткую мембрану.
- Если ненасыщенные жирные кислоты сжимаются, «изгибы» на их хвостах отталкивают соседние молекулы фосфолипидов, что помогает поддерживать текучесть мембраны.
- Соотношение насыщенных и ненасыщенных жирных кислот определяет текучесть мембраны при низких температурах.
- Холестерин действует как буфер, препятствуя снижению текучести при низких температурах и препятствуя увеличению текучести при высоких температурах.
Ключевые термины
- фосфолипид : любой липид, состоящий из диглицерида в сочетании с фосфатной группой и простой органической молекулой, такой как холин или этаноламин; они являются важными составляющими биологических мембран
- текучесть : мера степени текучести чего-либо.Величина, обратная его вязкости.
Текучесть мембраны
Есть несколько факторов, которые приводят к текучести мембраны. Во-первых, мозаичность мембраны помогает плазматической мембране оставаться жидкой. Интегральные белки и липиды существуют в мембране как отдельные, но слабо связанные молекулы. Мембрана не похожа на воздушный шар, который может расширяться и сжиматься; скорее, он довольно жесткий и может лопнуть, если в него проникнуть или если ячейка впитает слишком много воды. Однако из-за своей мозаичности очень тонкая игла может легко проникнуть в плазматическую мембрану, не вызывая ее разрыва; мембрана будет течь и самоуплотняться при извлечении иглы.
Текучесть мембраны : Плазматическая мембрана представляет собой жидкую комбинацию фосфолипидов, холестерина и белков. Углеводы, прикрепленные к липидам (гликолипидам) и белкам (гликопротеинам), выходят из обращенной наружу поверхности мембраны.
Второй фактор, который приводит к текучести, — это природа самих фосфолипидов. В своей насыщенной форме жирные кислоты в фосфолипидных хвостах насыщены связанными атомами водорода; между соседними атомами углерода нет двойных связей.В результате хвосты получаются относительно прямыми. Напротив, ненасыщенные жирные кислоты не содержат максимальное количество атомов водорода, хотя они действительно содержат некоторые двойные связи между соседними атомами углерода; двойная связь приводит к изгибу цепочки атомов углерода примерно на 30 градусов. Таким образом, если насыщенные жирные кислоты с их прямыми хвостами сжимаются при понижении температуры, они давят друг на друга, образуя плотную и довольно жесткую мембрану. Если ненасыщенные жирные кислоты сжаты, «изгибы» в своих хвостах отталкивают соседние молекулы фосфолипидов, сохраняя некоторое пространство между молекулами фосфолипидов.Это «локальное пространство» помогает поддерживать текучесть мембраны при температурах, при которых мембраны с хвостами насыщенных жирных кислот в их фосфолипидах «замерзают» или затвердевают. Относительная текучесть мембраны особенно важна в холодных условиях. Холодная среда имеет тенденцию сжимать мембраны, состоящие в основном из насыщенных жирных кислот, что делает их менее текучими и более восприимчивыми к разрыву. Многие организмы (например, рыба) способны адаптироваться к холоду, изменяя долю ненасыщенных жирных кислот в своих мембранах в ответ на понижение температуры.
У животных третьим фактором, удерживающим мембранную жидкость, является холестерин. Он находится рядом с фосфолипидами в мембране и имеет тенденцию ослаблять воздействие температуры на мембрану. Таким образом, холестерин действует как буфер, не позволяя более низким температурам препятствовать текучести и предотвращая чрезмерное повышение текучести при высоких температурах. Холестерин расширяет в обоих направлениях диапазон температур, при котором мембрана является соответственно текучей и, следовательно, функциональной.Холестерин также выполняет другие функции, такие как организация кластеров трансмембранных белков в липидные рафты.
Структура мембраны | Биология для майоров I
Описать структуру и функцию мембран, особенно бислоя фосфолипидов.
В результате мы узнаем о структуре мембран.
Цели обучения
- Опишите строение клеточных мембран
- Определить компоненты клеточной мембраны, включая фосфолипиды, холестерин, белки и углеводы
- Объясните, почему гидрофильные вещества не могут проходить сквозь клеточную мембрану
Структура клеточной мембраны
Плазматическая мембрана клетки определяет границу клетки и определяет характер ее контакта с окружающей средой.Клетки исключают одни вещества, поглощают другие и выделяют третьи в контролируемых количествах. Плазматические мембраны ограничивают границы клеток, но они не являются статическим мешком, а динамичны и постоянно находятся в движении. Плазматическая мембрана должна быть достаточно гибкой, чтобы определенные клетки, такие как эритроциты и лейкоциты, могли изменять форму при прохождении через узкие капилляры. Это наиболее очевидные функции плазматической мембраны. Кроме того, поверхность плазматической мембраны несет маркеры, которые позволяют клеткам узнавать друг друга, что имеет жизненно важное значение, поскольку ткани и органы формируются на раннем этапе развития, и которые позже играют роль в различении между «я» и «не-я». иммунный ответ.
Плазматическая мембрана также несет рецепторы, которые являются местами прикрепления определенных веществ, взаимодействующих с клеткой. Каждый рецептор устроен так, чтобы связываться с определенным веществом. Например, поверхностные рецепторы мембраны создают изменения внутри, такие как изменения ферментов метаболических путей. Эти метаболические пути могут иметь жизненно важное значение для обеспечения клетки энергией, выработки определенных веществ для клетки или расщепления клеточных отходов или токсинов для утилизации.Рецепторы на внешней поверхности плазматической мембраны взаимодействуют с гормонами или нейротрансмиттерами и позволяют передавать свои сообщения в клетку. Некоторые сайты распознавания используются вирусами как точки прикрепления. Хотя они очень специфичны, патогены, такие как вирусы, могут развиваться, чтобы использовать рецепторы для проникновения в клетку, имитируя конкретное вещество, которое рецептор должен связывать. Эта специфичность помогает объяснить, почему вирус иммунодефицита человека (ВИЧ) или любой из пяти типов вирусов гепатита проникает только в определенные клетки.
Жидкая мозаика Модель
В 1972 году С. Дж. Сингер и Гарт Л. Николсон предложили новую модель плазматической мембраны, которая, по сравнению с более ранним пониманием, лучше объясняла как микроскопические наблюдения, так и функцию плазматической мембраны. Это было названо моделью жидкой мозаики . Модель со временем несколько эволюционировала, но по-прежнему лучше всего объясняет структуру и функции плазматической мембраны в том виде, в котором мы их теперь понимаем. Модель жидкой мозаики описывает структуру плазматической мембраны как мозаику компонентов, включая фосфолипиды, холестерин, белки и углеводы, в которых компоненты могут течь и менять положение, сохраняя при этом базовую целостность мембраны.Как молекулы фосфолипидов, так и встроенные белки способны быстро и латерально диффундировать в мембрану (рис. 1). Текучесть плазматической мембраны необходима для активности определенных ферментов и транспортных молекул внутри мембраны. Плазменные мембраны имеют толщину от 5 до 10 нм. Для сравнения, красные кровяные тельца человека, видимые с помощью световой микроскопии, имеют толщину примерно 8 мкм, или примерно в 1000 раз толще плазматической мембраны.
Рис. 1. Жидкая мозаичная модель структуры плазматической мембраны описывает плазматическую мембрану как жидкую комбинацию фосфолипидов, холестерина, белков и углеводов.
Плазматическая мембрана состоит в основном из бислоя фосфолипидов со встроенными белками, углеводами, гликолипидами и гликопротеинами, а в клетках животных — холестерином. Количество холестерина в плазматических мембранах животных регулирует текучесть мембраны и изменяется в зависимости от температуры окружающей среды клетки. Другими словами, холестерин действует как антифриз на клеточной мембране, и его больше у животных, живущих в холодном климате.
Основная ткань мембраны состоит из двух слоев молекул фосфолипидов, и полярные концы этих молекул (которые выглядят как набор шариков в изображении модели художником) (рис. 1) находятся в контакте с водной жидкостью. внутри и снаружи клетки.Таким образом, обе поверхности плазматической мембраны гидрофильны («водолюбивы»). Напротив, внутренняя часть мембраны между двумя ее поверхностями представляет собой гидрофобную («ненавидящую воду») или неполярную область из-за хвостов жирных кислот. Эта область не имеет притяжения для воды или других полярных молекул (мы обсудим это далее на следующей странице).
Белки составляют второй по величине химический компонент плазматических мембран. Интегральные белки встроены в плазматическую мембрану и могут охватывать всю или часть мембраны.Интегральные белки могут служить каналами или насосами для перемещения материалов в клетку или из клетки. Периферические белки находятся на внешней или внутренней поверхности мембран, прикрепленные либо к интегральным белкам, либо к молекулам фосфолипидов. Как интегральные, так и периферические белки могут служить ферментами, структурными прикреплениями волокон цитоскелета или частью сайтов узнавания клетки.
Углеводы — третий важный компонент плазматических мембран. Они всегда находятся на внешней поверхности клеток и связаны либо с белками (образуя гликопротеины), либо с липидами (образуя гликолипиды).Эти углеводные цепи могут состоять из 2–60 моносахаридных единиц и могут быть прямыми или разветвленными. Наряду с периферическими белками углеводы образуют на поверхности клетки специализированные участки, которые позволяют клеткам узнавать друг друга.
Как вирусы заражают определенные органы
Рис. 2. ВИЧ стыкуется и связывается с рецептором CD4, гликопротеином на поверхности Т-клеток, перед тем, как проникнуть в клетку или инфицировать ее. (кредит: модификация работы Национальных институтов здравоохранения США / Национального института аллергии и инфекционных заболеваний)
Определенные молекулы гликопротеинов, экспонированные на поверхности клеточных мембран клеток-хозяев, используются многими вирусами для заражения определенных органов.Например, ВИЧ способен проникать через плазматические мембраны определенных видов белых кровяных телец, называемых Т-хелперами и моноцитами, а также через некоторые клетки центральной нервной системы. Вирус гепатита поражает только клетки печени.
Эти вирусы способны проникать в эти клетки, потому что клетки имеют сайты связывания на своей поверхности, которые вирусы использовали с одинаково специфическими гликопротеинами в их оболочках. (Фигура 2). Клетка обманывается имитацией молекул вирусной оболочки, и вирус может проникать в клетку.Другие сайты узнавания на поверхности вируса взаимодействуют с иммунной системой человека, побуждая организм вырабатывать антитела. Антитела вырабатываются в ответ на антигены (или белки, связанные с инвазивными патогенами). Эти же сайты служат местами для прикрепления антител и либо уничтожают, либо подавляют активность вируса. К сожалению, эти сайты на ВИЧ кодируются генами, которые быстро меняются, что очень затрудняет производство эффективной вакцины против вируса. Популяция вируса внутри инфицированного человека быстро эволюционирует посредством мутаций в разные популяции или варианты, различающиеся различиями в этих сайтах распознавания.Такое быстрое изменение вирусных поверхностных маркеров снижает эффективность иммунной системы человека при атаке вируса, поскольку антитела не распознают новые вариации поверхностных структур.
Фосфолипиды
Как мы только что узнали, основная ткань мембраны состоит из двух слоев молекул фосфолипидов. Гидрофильные или «водолюбивые» области этих молекул (которые выглядят как набор шариков в изображении модели художником) (рис. 1) находятся в контакте с водной жидкостью как внутри, так и снаружи клетки.Таким образом, обе поверхности плазматической мембраны гидрофильны. Напротив, внутренняя часть мембраны между двумя ее поверхностями представляет собой гидрофобную или неполярную область из-за хвостов жирных кислот. Эта область не имеет притяжения для воды или других полярных молекул (мы обсудим это далее на следующей странице).
Гидрофобные или ненавидящие воду молекулы, как правило, неполярны. Они взаимодействуют с другими неполярными молекулами в химических реакциях, но обычно не взаимодействуют с полярными молекулами.При помещении в воду гидрофобные молекулы имеют тенденцию образовывать шар или кластер. Гидрофильные области фосфолипидов имеют тенденцию образовывать водородные связи с водой и другими полярными молекулами как снаружи, так и внутри клетки. Таким образом, поверхности мембраны, обращенные внутрь и снаружи клетки, являются гидрофильными. Напротив, внутренняя часть клеточной мембраны гидрофобна и не взаимодействует с водой. Таким образом, фосфолипиды образуют превосходную двухслойную клеточную мембрану, которая отделяет жидкость внутри клетки от жидкости вне клетки.
Рис. 3. Эта молекула фосфолипида состоит из гидрофильной головки и двух гидрофобных хвостов. Гидрофильная головная группа состоит из фосфатсодержащей группы, присоединенной к молекуле глицерина. Гидрофобные хвосты, каждый из которых содержит насыщенную или ненасыщенную жирную кислоту, представляют собой длинные углеводородные цепи.
Молекула фосфолипида (рис. 3) состоит из трехуглеродного глицеринового остова с двумя молекулами жирных кислот, присоединенными к атомам углерода 1 и 2, и фосфатсодержащей группой, присоединенной к третьему атому углерода.
Такое расположение дает всей молекуле область, описываемую как ее голова (фосфатсодержащая группа), которая имеет полярный характер или отрицательный заряд, и область, называемую хвостом (жирные кислоты), которая не имеет заряда. Голова может образовывать водородные связи, а хвост — нет. Молекула с таким расположением положительно или отрицательно заряженной области и незаряженной или неполярной области называется амфифильной или «двоякой».
Эта характеристика жизненно важна для структуры плазматической мембраны, потому что в воде фосфолипиды имеют тенденцию располагаться так, чтобы их гидрофобные хвосты были обращены друг к другу, а их гидрофильные головки были обращены наружу.Таким образом, они образуют липидный бислой — барьер, состоящий из двойного слоя фосфолипидов, который отделяет воду и другие материалы на одной стороне барьера от воды и других материалов на другой стороне. Фактически, фосфолипиды, нагретые в водном растворе, имеют тенденцию спонтанно образовывать маленькие сферы или капли (называемые мицеллами или липосомами), причем их гидрофильные головки образуют внешнюю поверхность, а их гидрофобные хвосты — внутри (Рисунок 4).
Рис. 4. В водном растворе фосфолипиды имеют тенденцию располагаться так, чтобы их полярные головки были обращены наружу, а их гидрофобные хвосты были обращены внутрь.(кредит: модификация работы Марианы Руис Вильярреал)
Резюме: Структура клеточной мембраны
Современное понимание плазматической мембраны называется моделью жидкой мозаики. Плазматическая мембрана состоит из бислоя фосфолипидов с их гидрофобными хвостами жирных кислот, контактирующими друг с другом. Ландшафт мембраны усыпан белками, некоторые из которых покрывают мембрану. Некоторые из этих белков служат для транспортировки материалов в клетку или из клетки.Углеводы присоединяются к некоторым белкам и липидам на обращенной наружу поверхности мембраны. Они образуют комплексы, которые функционируют, чтобы идентифицировать клетку с другими клетками. Жидкая природа мембраны обязана конфигурации хвостов жирных кислот, присутствию холестерина, встроенного в мембрану (в клетках животных), и мозаичному характеру белков и комплексов белок-углевод, которые не закреплены прочно. место. Плазматические мембраны ограничивают границы клеток, но они не являются статическим мешком, а динамичны и постоянно находятся в движении.
Проверьте свое пониманиеОтветьте на вопросы ниже, чтобы увидеть, насколько хорошо вы понимаете темы, затронутые в предыдущем разделе. В этом коротком тесте , а не засчитываются в вашу оценку в классе, и вы можете пересдавать его неограниченное количество раз.
Используйте этот тест, чтобы проверить свое понимание и решить, следует ли (1) изучить предыдущий раздел дальше или (2) перейти к следующему разделу.
Альтернативы мембран в мирах без кислорода: создание азотосомы
Реферат
Двухслойная липидная мембрана, которая является основой жизни на Земле, нежизнеспособна вне биологии, основанной на жидкой воде.Этот факт побудил астрономов, которые ищут условия, подходящие для жизни, искать экзопланеты в «обитаемой зоне», узкой полосе, в которой может существовать жидкая вода. Однако могут ли клеточные мембраны быть созданы и функционировать при температурах намного ниже тех, при которых вода является жидкостью? Мы делаем шаг к ответу на этот вопрос, предлагая новый тип мембраны, состоящей из небольших органических соединений азота, способных образовываться и функционировать в жидком метане при криогенных температурах.Используя молекулярное моделирование, мы демонстрируем, что эти мембраны в криогенном растворителе обладают эластичностью, равной эластичности липидных бислоев в воде при комнатной температуре. В качестве доказательства концепции мы также демонстрируем, что стабильные криогенные мембраны могут возникать из соединений, наблюдаемых в атмосфере спутника Сатурна, Титана, известного наличием морей жидкого метана на его поверхности.
Ключевые слова- Титан
- абиогенез
- экзобиология
- липосома
- физическая химия
- квантовая химия
- вычислительная химия
- молекулярная динамика
ВВЕДЕНИЕ
Исследования протобиологии и образования клеток на Земле в основном сосредоточены на нуклеиновых кислотах; действительно, обычно считается, что рибонуклеиновые кислоты были предшественниками земной жизни (гипотеза «мира РНК») ( 1 ).Однако недавние исследования показали, что катализ РНК зависит от установления высоких локальных концентраций, а это означает, что компартментализация, вероятно, была такой же или более ранней фазой, чем РНК ( 2 ). Это подтверждает гипотезу «липидного мира», в которой липидные мембраны сыграли важную роль как очень ранний эволюционный шаг в создании жизни на Земле ( 3 ). Было обнаружено, что липидные бислои без дополнительных клеточных механизмов растут, делятся, способствуют реакциям полимеризации и даже синтезируют РНК из ферментов полимеразы ( 4 — 6 ).
Мембраны земных клеток состоят из бислоя фосфолипидов: поверхностно-активных веществ, состоящих из неполярных липидных цепей и насыщенных кислородом полярных головок. Полярные головки образуют поверхности, совместимые с водой, позволяя мембране разделять водный мир снаружи и водную жизнь внутри. Липидные хвосты фосфолипидов объединяются силами Ван-дер-Ваальса, таким образом стабилизируя мембрану. Везикула, состоящая из такой мембраны, называется липосомой.
Роль самоорганизующихся поверхностно-активных веществ в эволюционной биологии на Земле поднимает вопрос о том, могут ли неводные условия поддерживать какую-либо аналогичную структуру.Экспериментальные исследования были выполнены для создания везикул в неполярных растворителях. Это включало рассмотрение неионных простых эфиров ( 7 ), сложных эфиров ( 8 ), поверхностно-активных веществ ( 9 ) и инвертированных фосфолипидов ( 10 ). Обратные фосфолипидные мембраны даже рассматривались как биологические возможности в жидком метане ( 7 — 16 ).
Жидкий метан представляет особый интерес, потому что это единственная жидкость, кроме воды, которая образует моря на поверхности планетарного тела в нашей солнечной системе.Это тело — спутник Сатурна, Титан ( 11 , 12 ). Неизвестно, может ли Титан поддерживать любую форму клеточной мембраны. Однако мы действительно наблюдаем, что на поверхности Титана происходит неизвестный процесс, который потребляет водород, ацетилен и этан, которые постоянно стекают из атмосферы, но не накапливаются ( 13 — 15 ). Это делает жидкий метан очень интересным растворителем для использования в качестве альтернативы клеточной мембране.
Однако фосфолипидные мембраны, которые настолько прочны и эластичны в воде, не работают так хорошо в жидком метане.Неполярные хвосты фосфолипидов, казалось бы, совместимы с неполярным жидким метаном, а полярные головы друг с другом; Означает ли это, что в метане может существовать мембрана, обратная той, которая образовалась в воде? К сожалению нет; эта гипотеза фосфолипидов не учитывает тот факт, что хвосты фосфолипидов представляют собой длинноцепочечные углеводороды, которые будут жесткими при криогенных температурах. Кроме того, атомы фосфолипидного головного компонента, кислорода и фосфора, недоступны ни в какой форме в метановых морях Титана и, вероятно, ни в какой подобной среде жидкого метана.Следовательно, липосомы с обращенной фазой не являются жизнеспособным вариантом. Однако идея использования полярности для предотвращения растворения верна, если существуют какие-либо подходящие материалы.
В качестве доказательства концепции образования пузырьков в среде, богатой метаном, мы начали поиск полярных материалов, используя те, которые образуются естественным образом, когда ультрафиолетовый свет взаимодействует с атмосферой, содержащей метан и азот ( 12 ). Из спектроскопических наблюдений орбитального аппарата «Кассини» мы знаем наиболее распространенные полярные соединения в верхней части метано-азотной атмосферы Титана, как показано в таблице 1 [( 12 ), стр.167]. Ниже в атмосфере все эти виды конденсируются в аэрозоли, препятствуя дальнейшим наблюдениям с помощью Кассини. Лабораторные эксперименты по воспроизведению атмосферы метана и азота обычно дают смолистые остатки молекул, называемые толинами ( 17 ). Было обнаружено, что эти толины состоят из углеводородов, нитрилов и аминов ( 17 ). Поэтому мы также включили в наше исследование первичные нитрилы и амины длиной пропил-гексил, хотя содержание толинов относительно наблюдаемых Кассини видов остается неопределенным.
Таблица 1 Полярные соединения азота, обнаруженные на Титане, и их содержание в верхних слоях атмосферы, измеренное Кассини [( 12 ), стр. 167].Учитывая проблемы экспериментальных исследований при криогенных температурах, мы приняли подход молекулярного моделирования для отбора наиболее многообещающих кандидатов для самосборки в структуру, напоминающую мембрану. Мы рассматривали только короткие лиганды, учитывая тот факт, что более длинные лиганды не дают преимуществ при таких низких температурах. Все наши молекулы-кандидаты намного короче типичных фосфолипидов, которые включают углеродные цепи длиной от 15 до 20 атомов.Жидкий метан достаточно холоден, чтобы затвердеть практически любое вещество: четырехчленная углеродная цепь, например бутан, намного ниже точки замерзания, равной 133 К в жидком метане. При таких температурах может показаться почти невозможным формирование гибкой органической мембраны, не говоря уже о гибкости, подобной гибкости липидного бислоя. Однако низкая температура также позволяет небольшим молекулам агрегироваться иначе, чем при 300 К. Наша обычная интуиция должна быть приспособлена к более холодному миру.
Мы предположили, что мембраны жидкого метана будут полагаться на полярность азотсодержащих групп («азото»), чтобы удерживать их вместе, точно так же, как земные липосомы полагаются на неполярность алкильных групп. Поэтому мы назвали эти структуры «азотосомами». Сравнение липосом и предлагаемых структур азотосом показано на рис. 1.
рисунок 1 Липосомы и азотосомы.( A ) Липосома в полярном растворителе.Полярные головы скреплены неполярными липидными хвостами. ( B ) Азотосома в неполярном растворителе. Неполярные хвосты подпирают головы, богатые полярным азотом.
Ключевые физические требования к мембране заключаются в том, чтобы она была гибкой и стабильной. Наиболее распространенной мерой гибкости клеточной мембраны является модуль расширения площади K a (также известный как модуль расширения, растяжения или площади сжатия) ( 18 , 19 ). Модуль расширения площади мембран наземных клеток при комнатной температуре равен 0.От 24 до 0,50 Дж / м 2 ( 18 , 19 ). Как мы покажем, некоторые из наших кандидатов на азотосомы лежат в этом диапазоне. Наиболее распространенной мерой стабильности является шкала энергии разложения или времени стабильности ( 20 ). В целом липидные бислои на Земле метастабильны ( 21 ). Мы покажем, что некоторые из наших кандидатов на азотосомы имеют высокую энергию разложения по сравнению с криогенной средой, что приводит к очень длительным временным масштабам стабильности.
Синтез азотосом для экспериментального исследования будет сложным проектом, сродни первому синтезу липосом и дополнительным трудностям в криогенных условиях.Однако молекулы, из которых состоят азотосомы, похожи на молекулы, которые обычно изучаются на Земле, что делает свойства азотосом доступными с помощью стандартного молекулярного моделирования. Молекулярная динамика (МД) десятилетиями использовалась для моделирования двухслойных мембран ( 20 , 22 — 24 ) и полимерных везикул (полимерсом) ( 25 ). Было обнаружено, что значения K a , рассчитанные методом MD, хорошо согласуются с экспериментами ( 18 ), что подтверждает использование нами метода для этих новых мембран.
Чтобы обеспечить молекулярные силы в наших моделированиях, мы использовали Оптимизированные потенциалы для моделирования жидкостей (OPLS), которые являются хорошо известными и эффективными моделями для жидких углеводородов, малых органических молекул ( 26 , 27 ) и полимерсом ( 25 ). Мы подтвердили модели OPLS для наших молекул, подтвердив структуры, генерируемые OPLS, и парные энергии связи по сравнению с квантово-механическими расчетами ( 27 ), как описано в разделе «Материалы и методы».Только молекулы, которые OPLS точно моделировали с точки зрения длин связей, углов и энергий связи, были переданы для изучения в качестве кандидатов на азотосомы.
РЕЗУЛЬТАТЫ
Ошибки в моделях OPLS для длин связей, валентных углов и двугранных (торсионных) углов для тестируемых нами соединений представлены в таблице 2. Расчеты для трех наиболее высоконенасыщенных соединений — цианоацетилена, цианоаллена и 2,4-пентадииннитрила. — не рассматривались далее, потому что их модели OPLS показали ошибки в средней длине облигаций более 0.04 Å, что мы сочли недопустимо большим. Поскольку эти виды крайне ненасыщены, они с наименьшей вероятностью будут стабильными, когда они покинут верхние слои атмосферы, поэтому их непригодность для моделирования OPLS вряд ли будет иметь здесь значение. Для остальных соединений средняя разница между структурами OPLS и ab initio для длин связей составляла 0,008 Å, 0,6 ° в углах и 0,3 ° в диэдрах (если они есть).
Таблица 2 Ошибка в структурах, оптимизированных для OPLS.Средняя разница для каждого вида между его структурой OPLS и структурой, полученной с помощью ab initio оптимизации с моделью самосогласованного реакционного поля (SCRF) Онзагера для неявного растворителя.
Ab initio энергии связи были получены в вакууме и в неявном растворителе. Разница между этими энергиями составляла от 0,1 до 1,3 ккал / моль для всех оцениваемых веществ, в среднем 0,6 ккал / моль. Разница между энергиями связи OPLS и ab initio составляла от 0,2 до 0,9 ккал / моль, в среднем составляя 0,6 ккал / моль. В целом, значения энергии связи, генерируемой OPLS для данного вида, находятся между значениями ab initio с растворителем и без него, что поддерживает использование моделей OPLS.Можно ожидать, что энергии парной связи OPLS будут находиться между энергиями ab initio в вакууме и ab initio в растворителе, поскольку парные расчеты OPLS «подобны растворителям» из-за неполяризуемости модели OPLS. Это заставляет модель OPLS испытывать частичный эффект растворителя, даже когда присутствует только пара молекул. Особняком среди изученных нами молекул был HCN, энергия связи которого с OPLS была на 1,8 ккал / моль выше значения энергии связи, предсказанного ab initio представлением с неявным растворителем, что позволяет предположить, что модель OPLS для HCN неточна.
Однако, как мы покажем позже, HCN не самособирается в азотосому из-за своего небольшого размера. Таким образом, его чрезмерная энергия связи не будет иметь значения, потому что в дальнейшем он не будет рассматриваться из-за отсутствия самосборки. Энергии связи, найденные тремя методами (расчет OPLS и ab initio для системы в вакууме и растворителе), представлены в таблице 3.
Таблица 3 Парные энергии связи.OPLS и расчеты ab initio дали аналогичные результаты.
Каждая азотосома начинает моделирование как сетку молекул, а затем самоорганизуется в свою предпочтительную структуру.Виды, которые OPLS не мог точно представить, были исключены из рассмотрения, как и HCN, который не образовывал упорядоченный слой, и гексан, который образовывал твердое тело. Модули расширения площади оставшихся азотосом, а также простого бислоя гексана без функциональной головки показаны в таблице 4. Учитывая точность энергий связывания OPLS, мы ожидаем, что эти значения будут равны K a и ∆ E с точностью до 20%.
Таблица 4 Гибкость K нитрильных и аминных азотосом и энергия активации Δ E для удаления молекулы из каждой азотосомы.Все наши азотосомы обладают гибкостью, аналогичной гибкости известных мембран наземных клеток: от 0,13 до 0,55 Дж / м 2 для азотосом по сравнению с 0,24 до 0,50 Дж / м 2 для наземных липосом. Что касается тепловых колебаний, азотосомы будут казаться более жесткими, чем земные липосомы, потому что тепловые колебания на Титане меньше, чем на Земле. Однако в отношении механического стресса криогенные азотосомы и липосомы при комнатной температуре будут реагировать на удивление одинаково.
Поучительно сравнение гексана и гексаннитрила. Простой гексан образует слой в восемь раз более жесткий, чем гексаннитрил. Кроме того, бислой гексана является хрупким, как показано на рис. 2. После небольшого растяжения кажется, что он трескается. Напротив, слой гексаннитрила равномерно растягивается на всем протяжении. Единственное различие между этими двумя соединениями состоит в том, что гексаннитрил имеет полярную азотную головку.
Рис. 2 Растяжение азотосомы гексаннитрила и бислоя гексана.Наклон линейной посадки пропорционален модулю площади K a .
Ключевое различие между чистым углеводородным слоем и азотосомой заключается в структуре, обусловленной полярным азотным напором. Мы считаем, что именно эта структура позволяет криогенным азотосомам обладать гибкостью липидного бислоя при комнатной температуре.
Энергетические барьеры диссоциации для каждой азотосомы также приведены в таблице 4. Ацетонитрил, бутаннитрил, гексаннитрил, аминопропан и аминобутан имеют значения Δ E значительно ниже 8 ккал / моль, что указывает на нестабильные азотосомы.Азотосомы пропаннитрила, пентаннитрила, аминопентана и аминогексана имеют энергетический барьер, близкий к 8 ккал / моль. Их следует рассматривать в качестве возможных кандидатов, потому что их значения находятся в пределах 20% неопределенности, которая, как мы считаем, здесь уместна. Азотосомы акрилонитрила демонстрируют высокие барьеры разложения (17 ккал / моль), которые достаточны для обеспечения их стабильности в течение длительного времени.
Геометрия молекулы акрилонитрила, по-видимому, благоприятствует азотосомам и препятствует другим состояниям (рис.3). Это согласуется с тем фактом, что акрилонитрил, как экспериментально известно, имеет несколько неупорядоченную твердую фазу ( 28 ). Как и все азотосомы, изученные здесь, азотосомы акрилонитрила симметричны относительно плоскости мембраны, что означает, что, как и липидный бислой, они должны быть способны образовывать везикулы разных размеров.
Рис. 3 Состояния акрилонитрила.( A ) Азотосома. Связанные атомы азота и водорода укрепляют структуру.( B ) Твердый. Соседние атомы азота создают неблагоприятное отталкивание. ( C ) Мицеллы. Соседние атомы азота делают это крайне неблагоприятным. ( D ) Азотосомная везикула диаметром 90 Å, размером с небольшую вирусную частицу.
Расчет свободных энергий, необходимых для определения K a , также позволил нам получить полную свободную энергию разложения для каждой азотосомы. Эти значения показаны в Таблице 5. Все эти свободные энергии положительны, что указывает на то, что состояние азотосомы предпочтительнее растворенного состояния.Эти значения свободной энергии зависят от концентрации, потому что Δ G растворяется всегда отрицательно при бесконечном разбавлении. Концентрация, создаваемая растворением одной молекулы азотосомы в каждом боксе, составляет около 0,1%, что выше, чем мы могли ожидать в морях Титана. Однако реальные концентрации в настоящее время неизвестны, поэтому они могут быть или не быть достаточно высокими, чтобы сделать азотосомы термодинамически стабильными. В Δ G нет тенденции в отношении количества атомов углерода в цепи.Δ G , по-видимому, определяется тем, как молекулы подходят друг другу, а не каким-либо простым свойством самих молекул.
Таблица 5 Свободная энергия Гиббса разложения.Чистая механическая работа, необходимая для удаления молекулы с мембраны, с погрешностью 20%. Эти значения зависят от концентрации.
ОБСУЖДЕНИЕ
Мы предполагаем, что в холодном мире без кислорода пузырьки, необходимые для компартментализации, ключевого требования для жизни, будут сильно отличаться от пузырьков, обнаруженных на Земле.Вместо длинноцепочечных неполярных молекул, образующих прототип земной мембраны в водном растворе, мы находим мембраны, которые образуются в жидком метане при криогенных температурах, благодаря притяжению между полярными головками короткоцепочечных молекул, богатых азотом. Мы назвали такую мембрану азотосомой. Мы обнаружили, что гибкость таких мембран примерно такая же, как у мембран, образованных в водных растворах. Несмотря на огромную разницу в температурах между криогенными азотосомами и земными липосомами при комнатной температуре, которые делают почти любую молекулярную структуру жесткой, они демонстрируют удивительно и захватывающе похожие реакции на механическое воздействие.
На основании наших критериев термодинамической стабильности или, по крайней мере, метастабильности, азотосома кажется реализуемой криогенной мембраной. Исходя из всех известных молекулярных компонентов в атмосфере такого мира, Титана, мы смогли выбрать пару молекул-кандидатов, которые были способны проявлять свойства, которые, по-видимому, важны для образования пузырьков. Например, азотосома акрилонитрила имеет хорошую термодинамическую стабильность, высокий энергетический барьер для разложения и модуль расширения площади, аналогичный таковому у фосфолипидных клеточных мембран в богатых кислородом растворах.Акрилонитрил существует в атмосфере Титана в концентрации 10 частей на миллион и, вероятно, может образоваться на любом небесном теле с азотно-метановой атмосферой.
Наличие молекул, способных образовывать клеточные мембраны, само по себе не показывает, что жизнь возможна. Тем не менее, он направляет наши поиски на экзотические метаболические и репродуктивные химические процессы, которые были бы аналогичным образом совместимы в криогенных условиях. По мере того, как наше понимание условий, которые могут способствовать развитию внеземной жизни, расширяется, увеличивается и наша вероятность найти ее, возможно, в зоне обитания жидкого метана.
МАТЕРИАЛЫ И МЕТОДЫ
Первым свойством азотосом, которое мы исследовали, была их гибкость, измеренная по модулю расширения площади K a . Одной из процедур, которая использовалась для расчета этого свойства, является моделирование спонтанного колебания площади мембраны в течение длительного прогона МД ( 18 ). Однако этот метод основан на случайной выборке редких событий и, следовательно, имеет проблемы с точностью, завышая оценку K a в ≥2 раз ( 18 ).Вместо этого мы сделали мембрану заданным отступом и рассчитали модуль расширения площади, исходя из сопротивления растяжению ( 18 ). Это прямо сопоставимо с методом наноиндентирования, который используется для экспериментального нахождения K a , и сравнение такого моделирования и экспериментов с наземными липосомами показало, что они дают эквивалентные результаты ( 18 ).
Вторым критерием, который мы использовали для оценки азотосом, была их стабильность.Одна процедура, которая использовалась для изучения стабильности липосом, состоит в том, чтобы моделировать мембрану в течение длительного периода МД и наблюдать, диссоциирует ли она спонтанно ( 20 ). К сожалению, ожидание диссоциации эффективно только для самых слабых мембран, поскольку МД обычно охватывает только наносекунды моделируемого времени. Лучшая процедура — найти временной масштаб диссоциации по энергии активации ( 29 ). По закону Аррениуса скорость процесса с энергией активации Δ E пропорциональна exp (−Δ E / k B T ), где k B — постоянная Больцмана. а T — абсолютная температура ( 29 ).Если известен временной масштаб процесса без энергетического барьера, t 0 , то временной масштаб процесса с барьером определяется как t = t 0 exp (Δ E / к B T ).
Зависимость шкалы времени от Δ E является экспоненциальной, поэтому неопределенность шкалы времени будет больше, чем основная неопределенность энергетического барьера. К счастью, нам нужен только порядок величины шкалы времени.Для перемещения молекулы на 1 Å при 94 К без энергетического барьера требуется порядка t 0 = 1 пс. Если, например, требуется энергия активации 8 ккал / моль, это дает масштаб времени 1 пс × exp (8 ккал / моль / k B T ) = 235000 с (три земных дня). В отсутствие ошибки модели этот временной масштаб является достаточно длинным, чтобы можно было предположить, что азотосома достаточно стабильна, если ее энергетический барьер разложения превышает 8 ккал / моль.С погрешностью 20%, соответствующей погрешности между OPLS и ab initio энергиями связывания компонентов азотосом, более консервативным ограничением будет использование барьера в 10 ккал / моль, что соответствует времени разложения более 100 земных лет. .
Проверка силового поля OPLS
Мы подтвердили точность модели OPLS для наших молекул с помощью квантово-механических расчетов. Мы использовали программу квантовой механики Gaussian 09 с алгоритмом оптимизации Берни ( 30 ), используя уровень теории M062X / aug-cc-pVDZ и неявный углеводородный растворитель ( 31 ).Чтобы вычислить энергии связи, мы сравнили энергию оптимизированной свободно плавающей молекулы с энергией оптимизированной пары молекул. Для квантовой энергии связи мы исправили ошибку суперпозиции базисного набора по мере необходимости ( 32 ). Мы подтвердили структуры OPLS и парные энергии связи каждой из изученных здесь молекул в сравнении с этими квантово-механическими расчетами, и мы исключили любые модели OPLS, которые имели ошибки в расстояниях связей более 0,04 Å, в валентных углах (1 °), в двугранных координатах. углов (2 °) и энергий связи (1 ккал / моль).Двугранные, которые являются свободными роторами (например, вращение вокруг связи алканов C-C), не были включены в средние ошибки, поскольку их углы не вносят значительного вклада в энергию. Эти данные перечислены в результатах. Мы выполнили эти тесты, используя ab initio вычисления с вычислительно точным, но особенно точным уровнем теории M062X / aug-cc-pVDZ ( 33 ). Известно, что этот «миннесотский функционал» дает точные парные энергии связи для ван-дер-ваальсовых и полярных систем ( 34 ).
После подтверждения достоверности структур, созданных OPLS, с помощью моделирования ab initio, аналогичным образом были подтверждены и энергии связи. Для сравнения были созданы два набора энергий связи, генерируемых ab initio, один в вакууме и один в неявном растворителе. Энергии на основе растворителей ближе к экспериментальным условиям, тогда как энергии в вакууме использовались, по существу, как границы погрешности. Модели OPLS с ошибками энергии связи в растворителе более 1 ккал / моль были исключены.
Метод MD для гибкости мембраны
Чтобы найти гибкость и энергетические барьеры наших кандидатов в азотосомы, нам необходимо вычислить все возможные пути, по которым молекула может покинуть свою азотосому, а затем просуммировать соответствующие свойства этих маршрутов в соответствии с вероятностью их появления. Свойства, которые мы выбрали в качестве релевантных здесь, — это потенциальная энергия и сила, действующая на тестовую молекулу в направлении мембраны. Чтобы подготовить все эти возможные пути, мы начали с репрезентативного участка мембраны, сетки молекул размером 6 × 6 x — y для каждого вида-кандидата.
Затем этот кусок мембраны периодически расширяли, чтобы имитировать двумерную мембрану произвольной длины. Окружающее пространство было заполнено растворителем метаном. Краевые молекулы (те, для которых x = 0 или y = 0) удерживались фиксированными в направлении z , чтобы удерживать мембрану на месте. Мембране давали возможность уравновеситься, чтобы она самостоятельно собралась в желаемую структуру, как показано на рис. 4.
Рис. 4 Положения азотных головок в выбранных азотосомах.( A ) Начальная сетка. ( B ) Аминопентан (аморфный). ( C ) Пентаннитрил (гексагональный). ( D ) Акрилонитрил (гексагональная плотная упаковка).
Затем тестовая молекула (в местоположении x , y = 3,3) постепенно удалялась в направлении z . При каждом приращении тестовой молекуле позволяли свободно перемещаться в направлениях [ x , y ]. В направлении z он был слабо ограничен гармоническим потенциалом, что позволяло ему отбирать близлежащие местоположения z , но не покидать окрестности.Эта процедура, известная как «зонтичная выборка», позволяет производить выборку из всех возможных конфигураций, а также обеспечивает оценку того, была ли выборка адекватной — мы можем просто проверить, достаточно ли у нас выборок из каждого небольшого приращения в направлении z . Схема этого процесса представлена на рис. 5.
Рис. 5 Зонтичный отбор образцов процесса разложения азотосом.Тестовая молекула постепенно отводится от мембраны в направлении z .
Эта процедура необходима из-за высоких барьеров азотосом для разложения. Если бы барьеры для разложения были низкими, система, естественно, произвела бы выборку разложенных состояний в течение смоделированного времени. Зонтичная выборка вынуждает моделирование достичь этих состояний, даже если для их возникновения потребуется очень много времени из-за собственных флуктуаций.
На каждом из миллионов шагов МД оценивалась функция потенциальной энергии и вычислялась сила, необходимая для удержания тестовой молекулы от мембраны.В результате были получены профили силы и потенциальной энергии в зависимости от расстояния от мембраны, которые приводятся отдельно в дополнительных материалах. Профили силы были интегрированы по расстоянию, чтобы получить профили свободной энергии, как показано на рис. 6. Изменение площади было рассчитано путем измерения отклонения атома азота с выемкой в центре листа и определения площади образованной прямоугольной пирамиды. между ним и удерживаемым атомом азота по углам листа.Эта процедура оказалась очень устойчивой к изменениям общего размера листа. Отклонение зазубренного атома измерялось относительно равновесного состояния мембраны, то есть относительно точки минимума свободной энергии.
Рис. 6 Растяжение азотосом.Наклон аппроксимирующей линии пропорционален модулю площади K a .
Потенциальный энергетический барьер для каждой азотосомы был рассчитан путем обнаружения наибольшего разового непрерывного увеличения потенциальной энергии во время разложения каждой азотосомы.Концепция определяющего скорость энергетического барьера в стиле Аррениуса основана на непрерывности барьера. Если существует стабильное промежуточное состояние, при котором система может повторно уравновеситься, то это не один барьер, а два меньших барьера с резким увеличением предполагаемой скорости реакции. Поскольку мы использовали зонтичную выборку с ее детальным обзором энергетических профилей, мы смогли разделить их на очень мелкие участки (0,05 Å) и убедиться, что внутри наших барьеров нет промежуточных состояний.Пример барьера (акрилонитрил) показан на рис. 7.
Рис. 7 Профиль потенциальной энергии разложения акрилонитрила.Самый большой мгновенный энергетический барьер — это энергия активации разложения азотосомы.
Некоторые из мелких срезов 0,05 Å, почти все в начале и конце, где не могло произойти перекрытие зонтичного отбора проб, содержали менее 500 образцов. Мы удалили эти участки для рассмотрения как барьеры, потому что (500 образцов) × (2 фс на образец) меньше, чем временной масштаб нашего уравновешивания NPT (1000 фс).В результате наши расчеты энергетического барьера становятся более консервативными, поскольку частота дискретизации участка обратно пропорциональна его энергии.
Все прогоны МД были выполнены с использованием крупномасштабного атомно-молекулярного массивно-параллельного симулятора (LAMMPS; распространение март 2014 г.) ( 35 ). Стандартные параметры OPLS использовались без изменений из наборов данных Jorgensen 2008 ( 36 ). Были соблюдены типичные передовые методы моделирования мембран с помощью МД. Например, ансамбль постоянной температуры и постоянного давления (NPT) был применен с использованием термостата Носа-Гувера и баростата, причем баростат был анизотропным ( 37 ).Анизотропный баростат позволяет мембране свободно изменять или терять свою структуру, повышая реалистичность моделирования ( 20 ). Температура была установлена на 94 К, а давление на 1,45 атм, аналогично условиям на поверхности Титана ( 17 ). Использовалось интегрирование Верле с шагом по времени 2 фс ( 37 ). Алгоритм «частица-частица-сетка» использовался для добавления дальнодействующих кулоновских взаимодействий, которые важны при моделировании мембран ( 38 ).Короткодействующие силы, кулоновские взаимодействия и силы Леннарда-Джонса вычислялись попарно с радиусом отсечки 8 Å ( 38 ). Каждая мембрана была инициализирована как плоская плоскость x — y с периодическими граничными условиями в x , y и z , как показано на рис. 3. Начальный размер ячейки моделирования составлял 21 × 21 × 42 Å. Положение тестируемой молекулы изменяли с шагом 0,2 Å, начиная с 2 Å ниже ее начального положения в мембране и заканчивая на 10 Å выше, что дает 60 имитаций для каждого тестируемого вида.Затем сбор данных выполнялся в течение 1 нс на каждом приращении. Направление z на каждую молекулу оказывалось на ее концевой атом азота или, в неполярной молекуле, на ее концевой атом углерода. Это позволяло каждой молекуле вращаться, если она испытывала асимметричную силу, давая ей доступ к максимальному количеству степеней свободы. Ограничения на краевые молекулы были абсолютными ( z сил были установлены равными нулю), тогда как ограничение на тестовую молекулу было наложено как гармоническая сила с жесткостью упругости 10 ккал / моль-Å.Это умеренное ограничение позволило исследуемой молекуле покрыть диапазон 0,2 Å и перекрываться с диапазонами других симуляций, обеспечивая непрерывный анализ свойств системы.
Исправление (25 марта 2015 г.): Обновлен раздел благодарностей.
Это статья в открытом доступе, распространяемая в соответствии с условиями некоммерческой лицензии Creative Commons Attribution, которая разрешает использование, распространение и воспроизведение на любом носителе, при условии, что конечное использование не преследует коммерческих целей и при условии, что оригинальная работа правильно процитировано.
ССЫЛКИ И ПРИМЕЧАНИЯ
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- 11 116
- E. Lellouch, TE Cravens, Titan: Interior, Surface, Atmosphere, and Space Environment (Cambridge University Press, Кембридж, Великобритания, 2014), т. 14.
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
W.Йоргенсен, Всеатомные параметры OPLS для органических молекул, ионов, пептидов и нуклеиновых кислот (Йельский университет, Нью-Хейвен, Коннектикут, 2009).
- ↵
- ↵
- Авторские права © 2015, Авторы
Клеточная мембрана
Клеточная мембранаОсновным компонентом клеточной мембраны является двухслойный фосфолипид или сэндвич. Головки (часть фосфо ) полярны, а хвосты (часть липид ) неполярны.Головки, которые образуют внешнюю и внутреннюю облицовку, являются «гидрофильными» (водолюбивыми), в то время как хвосты, обращенные внутрь клеточной мембраны, являются «гидрофобными» (водобоязненными). Вода притягивается к внешней стороне (красный) мембраны, но не может пройти через неполярный внутренний (желтый) слой.
Транспортировка через мембрану
Мембраны клетки полупроницаемые. Это означает, что, хотя большинство вещей фактически сохраняется (или выключается), некоторые могут проходить напрямую.Так как же клетки перемещают предметы внутрь и наружу? Есть три метода.
1. Диффузия : Если молекула очень мала, например, кислород или углекислый газ, диффузия делает свое дело. Когда концентрация O 2 вне клетки выше, чем внутри, молекулы O 2 диффундируют внутрь, проходя через мембрану, как будто ее там даже нет. Точно так же, когда концентрация отработанного газа CO 2 увеличивается внутри электролизера, он естественным образом уходит наружу, где концентрация ниже.Для диффузии клетка не требует затрат энергии. Это происходит пассивно. Природа поняла это давным-давно, но сейчас мы производим ткани и медицинские устройства, которые копируют этот процесс. Gore Industries, один из крупных работодателей во Флагстаффе, производит ткань под названием «Gore-Tex», которая отталкивает крупные капли воды, но пропускает более мелкие молекулы воздуха, что делает ткань «дышащей».
Уловка: хотя диффузия хорошо работает для крошечной одиночной клетки, сама по себе она не выполняет свою работу в многоклеточном организме, где ткани находятся глубоко внутри тела.Представьте себе бицепс, когда вы поднимаете тяжести. Ткань, состоящая из миллионов клеток, быстро исчерпает кислород и накапливает углекислый газ. Распространение через кожу не могло угнаться. Здесь выручает кровеносная система. Через эти ткани проходят мельчайшие кровеносные сосуды, капилляры. Кровь из легких выделяет кислород клеткам (потому что O 2 находится в более низкой концентрации в тканях) и поглощает углекислый газ (потому что CO 2 находится в более высокой концентрации в тканях) и переносит его обратно в ткани. легкие на выдохе.Этот не требует энергии . Это также объясняет, почему частота вашего дыхания увеличивается, когда вы напрягаетесь, и является одной из причин, по которым вы должны быть многоклеточными.
2. Активный транспорт : Иногда диффузия не происходит достаточно быстро для нужд клетки, и бывают моменты, когда питательные вещества необходимо накапливать или выводить из организма в более высокой концентрации, чем это могло бы произойти естественным путем путем диффузии. В этом случае клетка использует энергию, чтобы перекачивать хорошее и плохое через белковые каналы или ворота.Этот процесс называется активным транспортом.
3. Эндоцитоз : Иногда нужно переместить большой объект внутрь или из камеры, но он слишком велик для двери. Подумайте о том, чтобы перенести диван в свою квартиру, и вы поймете идею. Но вы не можете просто вырезать отверстие в клеточной мембране, иначе все хорошее внутри вытечет наружу, так как же вы втянуть что-то, не позволяя своему внутреннему миру открываться внешнему виду? У клетки есть особый прием, который, вероятно, восходит к тем временам, когда вся жизнь была одноклеточной, и именно так клетки питались.Одноклеточная амеба Amoeba по-прежнему потребляет пищу таким образом. Это называется эндоцитоз, и работает он вот так. В частности, обратите внимание на то, что поглощенный продукт питания постепенно заключен в «вывернутую наизнанку» секцию двухслойной мембраны в стиле Pac-Man! Как только частица пищи полностью окружена, внешние мембраны сливаются, а внутренняя вакуоль отщипывается. Благодаря этому методу внутренняя часть клетки никогда не подвергается прямому воздействию внешней среды. Одним из побочных эффектов этого трюка является то, что мембрана теперь вывернута наизнанку, и это интересно, потому что дает нам представление о происхождении клеточных органелл.
Обратите внимание, что мембраны вакуоли перевернуты! (Черный снаружи и красный внутри)
В Биологический проект > Cell Биология > Клетка Мембраны > Обзор Клеточные мембраны: Основные понятия Графика модели жидкой мозаики для клеточной мембраны
задача 1 В Биологический проект > Cell Биология > Клетка Мембраны > Обзор http: // www.biology.arizona.edu |
Пространственное моделирование интерфейса мембрана-цитозоль в передаче сигнала протеинкиназы
Образец цитирования: Giese W, Milicic G, Schröder A, Klipp E (2018) Пространственное моделирование интерфейса мембрана-цитозоль в передаче сигнала протеинкиназы. PLoS Comput Biol 14 (4): e1006075. https: // doi.org / 10.1371 / journal.pcbi.1006075
Редактор: Йенс Нильсен, Технологический университет Чалмерса, ШВЕЦИЯ
Поступила: 10.10.2017; Одобрена: 7 марта 2018 г .; Опубликовано: 9 апреля 2018 г.
Авторские права: © 2018 Giese et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в документе и его файлах с вспомогательной информацией.
Финансирование: Эта работа была поддержана грантом Немецкого исследовательского фонда (CRC 740 «От молекул к модулям») EK. GM и AS выражают признательность за поддержку исследовательской программе Sparkling Science Федерального министерства науки, исследований и экономики Австрии (BMWFW) в рамках проекта Sparkling Science «EMMA {Эксперименты с математическими алгоритмами}» (SPA 05/172).Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Введение
Клеткам необходимо реагировать на широкий спектр внешних стимулов, таких как изменения окружающей среды или внеклеточные коммуникационные сигналы. Сигналы, передаваемые от рецепторов клеточной поверхности к генам-мишеням в ядре, часто передаются каскадами ковалентных модификаций белков.Эти модификации состоят из взаимопревращаемых форм белка, например, фосфорилированного и нефосфорилированного белка. Сигнальные каскады встречаются во многих различных вариантах, включая каскады митоген-активируемой протеинкиназы (MAPK) и небольшие каскады GTPase.
Механизмы передачи сигналов, осуществляемые сетями белок-белковых взаимодействий, очень модульны, а регуляторное поведение возникает из относительно простых модификаций [1]. Пространственное расположение сигнальных каскадов варьируется в разных биологических системах.Мы фокусируемся на локализации сигнальных компонентов, которые могут быть привязаны к клеточной мембране или свободно диффундировать в цитозоле. Привязка сигнальных молекул к клеточной мембране может быть опосредована модификациями липидирования [2–6], совместной локализацией с помощью мембраносвязанных каркасов [7] или белков, закрепляющих мембраны [8]. Часто первые шаги передачи сигнала происходят на мембране, а затем продолжаются в цитозоле. Мы исследуем каскады линейной передачи сигналов с различными реализациями пространственного расположения компонентов передачи сигналов, как показано на рисунке 1.Здесь мы сосредотачиваемся на интерфейсе мембрана-цитозоль, который включен в сигнальный мотив, показанный на Рис. 1 (B) и 1 (C).
Рис. 1. Пространственная организация сигнальных каскадов.
( A ) Эскиз классической модели временной передачи сигнала. Распространение этой модели на трехмерное пространство естественным образом приводит к появлению множества различных пространственных мотивов. ( B ) Сигнал сначала обрабатывается сигнальными компонентами, привязанными к мембране, а затем трансдуцируется на границе раздела мембрана-цитозоль в цитозоль.( C ) Компоненты передачи сигналов непосредственно активируются на границе раздела мембрана-цитозоль и диффундируют через цитозоль. Обратите внимание, что коэффициенты диффузии для боковой диффузии вдоль мембраны намного ниже, чем в цитозоле.
https://doi.org/10.1371/journal.pcbi.1006075.g001
Во многих экспериментальных и теоретических исследованиях сигнальных каскадов клетка рассматривается как ряд хорошо перемешанных компартментов без изменений в размере, форме или органеллах. расположение.Попытки количественного описания сигнальных каскадов с акцентом на временные аспекты были сделаны в [9–12]. Однако пространственному описанию сигнальных процессов уделялось меньше внимания, несмотря на его важность для понимания морфологии клеток и регуляции роста во времени и пространстве [13]. Примеры пространственных эффектов в масштабе длины отдельных клеток варьируются от процесса спаривания дрожжей [14, 15] до распространения пространственной информации в нейронах гиппокампа, которая контролируется формой клеток и наоборот [16, 17].
Поскольку цитозоль масштабируется вместе с объемом клетки, а клеточная мембрана — с площадью поверхности клетки, реакции на мембране и в масштабе цитозоля зависят от отношения поверхности клетки к объему клетки. Например, мы получаем отношение площади к объему 3/ R ячейка для сферической геометрии ячейки, где R ячейка — это радиус ячейки. Мы покажем, что это масштабирование влияет на общую скорость фосфорилирования сигнальных белков, которые диффундируют в цитоплазматическом объеме, который зависит от размера клетки.В то время как цитозольные градиенты естественным образом возникают от мембраны к ядру, связанные с мембраной компоненты могут образовывать градиенты только вдоль мембраны, что изменяет ответ на гетерогенные сигналы. Более того, диффузия на мембрану компонентов, связанных с мембраной, происходит намного медленнее, чем для цитозольных компонентов [18]. Ожидается, что оба эти фактора в значительной степени изменят свойства сигнальной трансдукции пути.
Анализ и сравнение пространственных мотивов передачи сигналов в ответ на пространственно однородные и гетерогенные сигналы представлены в этом исследовании.Естественным продолжением широко распространенных обыкновенных дифференциальных уравнений являются уравнения в частных производных с объемной поверхностью [19, 20]. Здесь основной объем относится к клеточным компартментам, которые представлены в виде объема, такого как цитоплазма или ядро, тогда как поверхность , относится ко всем клеточным структурам, которые представлены в виде области, такой как клеточная или ядерная мембрана. С момента своего появления в клеточных сигнальных системах [21] уравнения в частных производных с объемной поверхностью успешно применялись в нескольких моделях поляризации клеток [18, 22–24].Однако интерфейсы мембрана-цитозоль на разных стадиях сигнального каскада еще не исследованы.
Мы начинаем с анализа двух различных мотивов с упрощенной линейной кинетикой, которая позволяет разработать точные аналитические решения для стационарного состояния. Оба мотива различаются по зависимости от размера клеток, и мы далее показываем, что их поведение может радикально отличаться от предположения о хорошо смешанных компартментах. Масштабирование передачи сигнала по времени исследуется методом локальных времен накопления [25].Мы продолжаем исследовать реакцию и чувствительность к пространственно неоднородным сигналам, таким как сигнальные градиенты для симметричных и асимметричных форм клеток. В последнем разделе мы продолжаем численные исследования систем с отрицательными обратными связями, которые приводят к колебаниям, зависящим от размера ячейки. Анализ Фурье во времени используется для понимания зависимости частоты и амплитуды колебаний от размера ячейки. В зависимости от пространственного мотива получены пределы размера клетки для подавления колебательного поведения.
Мы начинаем с линейного сигнального каскада с различными локализациями мембранно-цитозольного интерфейса, как показано на рис. 1. Мы используем простую каскадную модель из [9], в которой стимуляция рецептора приводит к последовательной активации нескольких последующих протеинкиназы. Эта модель расширяется в космос следующим образом. Мы предполагаем линейный каскад с компонентами N , где первые компоненты M < N локализованы на мембране, в то время как остальные компоненты N — M предположительно свободно диффундируют в цитозоле.Уравнения для мембраносвязанных компонентов читаются следующим образом: (1) Здесь — локальные концентрации сигнальных молекул на клеточной мембране. Предполагается, что скорость активации первого компонента сигнализации зависит от входного сигнала, который обозначен. Входной сигнал на клеточной поверхности может быть триггером на клеточной мембране или возникать из внеклеточного сигнала. Все эти виды являются функциями пространства и времени, где — точка на мембране, а t — время. Диффузия вдоль клеточной мембраны, которая, как предполагается, представляет собой двумерную изогнутую поверхность в трехмерном пространстве, описывается оператором Лапласа-Бельтрами Δ Γ и коэффициентом диффузии D mem .Поскольку мембрана представляет собой поверхность в трехмерном пространстве с незначительной толщиной, естественной единицей для концентраций видов, связанных с клеточной мембраной P n ( n = 1,…, M ), является молекул на площадь. Молекулярные концентрации сигнальных молекул часто указываются в наномолярных или микромолярных (нМ или мкМ М). Поэтому для удобства мы используем единицы наномолярного или микромолярного временного микрометра ( n M мкм или мкм M мкм ) для мембраносвязанных сигнальных молекул.Отметим, что 1 мкм M мкм м ≈ 602 мол / мкм 2 .
Скорости фосфорилирования, а также скорости дефосфорилирования выражаются в единицах молекул на площадь и время. Если входной сигнал однороден в пространстве, то есть все пространственные потоки D mem ∇ Γ P n равны нулю, и система уравнений для мембраносвязанных видов может быть описана эквивалентным система обыкновенных дифференциальных уравнений (Приложение S1).В отличие от связанных с мембраной сигнальных компонентов P 1 ,…, P M , сигнальный компонент P M +1 может свободно диффундировать в цитозоле. Для моделирования интерфейса мембрана-цитозоль нам необходимо включить диффузию в цитозоле и реакции на его границах, которые являются мембранами. Эти процессы моделируются уравнением реакции-диффузии (2) с граничным условием (3) Поскольку P M +1 активируется расположенным выше по потоку компонентом P M , который привязан к мембране, реакция фосфорилирования происходит только на клеточной мембране, но не внутри нее. цитозоль.Таким образом, эта реакция моделируется как граничное условие. Реакции на границе раздела мембрана-цитозоль описываются скоростью фосфорилирования и скоростью инактивации v i , как в единицах молекул на площадь, так и во время. Вид P M +1 свободно диффундирует в цитозольном объеме со скоростью диффузии D cyt , и поэтому его локальная концентрация описывается в единицах молекул на объем.Скорость дефосфорилирования в цитозоле указывается в молекулах на объем и время. Обратите внимание, что скорость инактивации и v i могут быть вызваны мембраносвязанными фосфатазами или насыщением фосфорилирования на мембране. Оба, v a и v i , составляют кинетику на границе раздела мембрана-цитозоль. Для потока на всех других органеллах, заключенных в мембрану, мы предполагаем условие нулевого потока. (4) Уравнения для компонентов нижележащего цитозольного каскада читаются (5) Концентрации цитозольных компонентов в положении в цитозольном объеме в момент времени t описываются функциями с n = M + 1,…, N .Для цитозольных компонентов мы предполагаем условия нулевого потока: (6) (7) В классических каскадах MAPK последний компонент каскада, который представляет собой фосфорилированный MAPK, импортируется в ядро. Примеры варьируются от ядерного импорта Hog1 в дрожжах [26, 27] до импорта ERK у млекопитающих [28]. В этом случае граничное условие (7) на ядре для последнего цитозольного компонента P N необходимо изменить на (8) где ϵ представляет собой скорость реакции ядерного импорта на ядерной мембране.Если не указано иное, в данной статье предполагается, что ядро имеет граничное условие нулевого потока.
Мы протестируем и сравним системы с тремя компонентами N = 3, как показано на рис. 1, где пространственное расположение компонентов варьируется. Здесь M = 2 описывает случай двух мембраносвязанных и одного цитозольного элемента (мотив фиг. 1B), а M = 0 — случай только цитозольных компонентов (мотив фиг. 1C). В следующем случае M = 2 упоминается как смешанный мембранно-цитозольный (MMC) и M = 0 как чистый цитозольный (PC) каскад.
Результаты
Смешанный мембранно-цитозольный каскад сильно зависит от размера
Мы начинаем этот раздел с анализа сферической ячейки, а затем обобщаем анализ на ячейки произвольной формы. В дальнейшем предполагается сферическая ячейка радиуса R ячейка со сферическим ядром радиусом R nuc , расположенная в центре ячейки.
Входной сигнал обозначается P 0 ( t ) и предполагается однородным на поверхности ячейки.Концентрации протеинкиназ описываются функциями P i ( r , t ) в зависимости от пространства и времени. Обратите внимание, поскольку клеточная геометрия радиально симметрична и входной сигнал P 0 действует на клеточную мембрану однородно, эти функции зависят только от радиального расстояния от центра клетки, обозначенного r , и времени t . . В следующем анализе кинетические скорости линеаризованы, что означает, что мы предполагаем и для фосфорилирования и дефосфорилирования, соответственно.Скорость инактивации v i на границе мембрана-цитозоль также линеаризована с помощью v i = γP M +1 . Обратите внимание, что кинетика интерфейса может быть переформулирована как, из чего легко увидеть, что активация на мембране насыщается при. Уравнения модели для смешанного мембранно-цитозольного каскада (MMC) с линеаризованной кинетикой читаются следующим образом: (9) (10) (11) и граничные условия для цитозольных видов P 3 : (12) (13)
Существует несколько оценок активности фосфатазы и коэффициентов диффузии для сигнальных компонентов MAPK.Коэффициент диффузии, D cyt , глобулярных цитозольных белков находится в диапазоне 1-10 мкм 2 s -1 , в то время как коэффициент диффузии мембраносвязанных компонентов D mem , намного ниже со значением в диапазоне 10 −3 — 0,1 мкм 2 s −1 [29–31]. Скорости фосфатазы β n колеблются более трех порядков величины 0.1 — 100 с -1 [32, 33]. В случае Fus3, который является MAPK в пути спаривания дрожжей S. cerevisiae , коэффициент диффузии и скорость цитозольного дефосфорилирования были оценены как 4,2 мкм 2 s -1 и 1 с −1 соответственно [14]. См. Таблицу 1 для обзора значений параметров и единиц измерения.
Мы начинаем с анализа стационарного состояния этой системы в интересующих параметрах режимах и предполагаем, что сигнал P 0 является постоянным во времени.Здесь и далее мы обозначаем устойчивое распределение полосой, что означает устойчивое состояние P n . Устойчивое состояние первых двух элементов определяется как и. Для установившегося состояния P 3 решение дается формулой (14) где i 0 и k 0 — модифицированные сферические функции Бесселя первого и второго рода соответственно [37]. Обратите внимание, что i 0 увеличивается с r (расстояние от центра ячейки), а k 0 является убывающей функцией r .Коэффициенты A и B выведены в Приложении S1. Если мы пренебрегаем ядром или в цитозоле нет ядра, то есть R nuc = 0, коэффициент B становится равным нулю. Устойчивое решение для различных размеров ячеек показано на рис. 2.
Рис. 2. Профили внутриклеточной концентрации для двух различных мотивов передачи сигнала.
( A ) Концентрация третьего каскадного элемента P 3 была нанесена на срез через трехмерные ячейки различного размера.Цифры над ячейками указывают их радиус. Внутриклеточные градиенты более крутые для каскада MMC [верхний ряд], чем для каскада ПК [нижний ряд]. Использованные параметры: α 1 = α 2 = α 3 = 1,5 с −1 , β 1 = β 2 = β 3 = 1,0 с -1 , D mem = 0,03 мкм 2 с -1 , D cyt = 3.0 мкм 2 с -1 , γ = 10,0 мкм с -1 , P 0 ≡ 100 n M мкм . ( B ) Зависимость каскада ММС от размера с двумя мембраносвязанными и одним цитозольным типами. ( C ) Размерная зависимость каскада ПК. Ядерная мембрана обозначена пунктирной линией.
https://doi.org/10.1371/journal.pcbi.1006075.g002
Концентрация максимальна на клеточной мембране и уменьшается по направлению к ядру.Оценка длины распада L градиента внутриклеточного градиента (с максимальной концентрацией на мембране) дается [32]. Эту длину затухания можно сравнить с фактическим размером ячейки. Их отношение называется модулем Тиле, безразмерной мерой, определяемой как [33]. Для Φ 1 следует ожидать сильных внутриклеточных градиентов и неоднородностей концентраций сигнальных молекул, тогда как для Φ ≪ 1 концентрация почти однородна. Поскольку модуль Тиле связывает коэффициент диффузии и скорость деградации с размером клетки, это важный параметр для исследования формирования градиента [33] и распространения сигнала для нескольких каскадных уровней [38].Однако в трехмерном пространстве L градиент больше не может интерпретироваться как фактический градиент, поскольку его вывод основан на предположении об одномерной геометрии. Кроме того, если предполагается исключительный объем, такой как ядро, одномерный градиент L завышает градиент концентрации. Например, если принять D cyt = 4,0 мкм 2 / s и β = 1.0 с −1 , получаем L градиент = 2,0 мкм . В случае классического одномерного упрощения предполагается распад, пропорциональный ∝ exp (- x / L градиент ), что предполагает уменьшение концентрации на расстоянии x = 2 мкм на коэффициент exp (- x / L градиент ) ≈ 0,37. Однако в сферической ячейке с радиусом R ячейка = 3 мкм с исключенным объемом R nuc = 1 мкм концентрация уменьшается только в 0 раз.77 на расстоянии 2 мкм от клеточной мембраны. Влияние размера клетки на градиенты внутриклеточной концентрации показано на рис. 2.
Зависимость размера клетки в сигнальных системах клетки возникает не только из-за характерного масштаба длины для формирования внутриклеточного градиента, но и из-за изменения средних уровней внутриклеточной концентрации с размером клетки. Мы начинаем с упрощающего предположения, что в цитозоле нет ядра или исключающего объема, что означает R nuc = 0.В этом случае стационарное решение читается как (15) Модифицированные сферические функции Бесселя i 0 и i 1 являются монотонно возрастающими функциями с и. Мы получаем для клеток с малым Φ и, следовательно, реакция фосфорилирования на мембране в этом случае идет при насыщении. Для больших Φ получаем из нижней оценки. Эти оценки справедливы и в случае исключающего объема, которым является ядро, и мы получаем оценку концентрации на клеточной мембране: (16) Зависимость абсолютных уровней концентрации от границы раздела мембрана-цитозоль показана на рис. 2 и 3 для набора различных параметров.При большой скорости инактивации на границе раздела мембрана-цитозоль зависимость размера клеток уменьшается. Следовательно, зависимость размера клеток в основном определяется γ и не зависит от скорости фосфорилирования α .
Рис. 3. Зависимость уровней концентрации от размера и формы клеток.
Средняя концентрация третьего каскадного элемента на клеточной мембране [первая строка], в цитозоле [вторая строка], в ядре [третья строка], а также нормализованная дисперсия [четвертая строка] была нанесена на график относительно клетки. диаметр d x .При изменении d x формы ячеек были пропорционально масштабированы по оси y и z. Использовались следующие параметры: α 1 = α 2 = α 3 = 1,5 с −1 и β 1 = β 2 = β 3 = 1,5 с -1 , D mem = 0,03 мкм 2 с -1 , D cyt = 3.0 мкм 2 s -1 и P 0 ≡ 100 n M мкм . Моделирование каскада MMC [точки] и [крестики] было выполнено для γ = 0 [синий и красный], а также γ = 1,0 мкм s -1 [оранжевый и зеленый]. Средняя концентрация в цитозоле абсолютно одинакова для обоих каскадов [второй столбец]. Для всех форм средняя концентрация точно аппроксимируется Λ 3 (MMC) или (PC), а для γ = 1.0 мкм с -1 аппроксимация слегка завышает среднюю концентрацию (пунктирная линия).
https://doi.org/10.1371/journal.pcbi.1006075.g003
Мы можем продолжить исследование эволюции средних уровней концентрации, которая зависит от концентрации на клеточной мембране и силы внутриклеточного градиента. В случае произвольной формы ячеек с объемом ячейки V ячейкой и площадью клеточной мембраны M ячейкой средняя концентрация получается из (17) В [33] аналитические решения для средней концентрации в сферической ячейке и пластине были получены как функции модуля Тиле.Однако, поскольку выводы ограничены геометрией клеток, где доступно явное аналитическое решение уравнения реакции диффузии, мы вводим альтернативный подход для оценки средних уровней концентрации в зависимости от цитозольного объема и площади клеточной мембраны. Поскольку сигнал распространяется от клеточной мембраны в цитозоль, клеточную мембрану можно рассматривать как источник, в то время как цитозольный объем, в котором фосфорилированные сигнальные молекулы дефосфорилируются, можно рассматривать как сток.Эта идея может быть получена математически путем интегрирования уравнения (2) и применения теоремы Грина, что приводит к (18) Здесь продукция в левой части уравнения зависит от площади клеточной мембраны, которая уравновешивается деградацией в цитозоле в правой части уравнения. На основе уравнения сохранения массы (см. Приложение S1) в реакционно-диффузионных системах мы вводим следующую меру: (19) Эта мера имеет свойство γ = 0 или β = 0, что справедливо для произвольной формы ячеек.Кроме того, для сферической ячейки оценка верна для β > 0 и γ > 0 (см. Приложение S1 и рис. 3). Поэтому мы используем Λ M +1 в качестве заместителя для средней концентрации для произвольных форм ячеек, которую можно легко вычислить.
Сравнение оценки Λ 3 со средней концентрацией показано на рис. 3 для различных форм ячеек, которые представляют собой сферическую ячейку, ячейку в форме стержня, ячейку с одним выступом и ячейку с двумя выступами.Эти формы клеток встречаются, например, у S. cerevisiae , S. pombe и гаплоидных S. cerevisiae , стимулированных феромоном спаривания [39, 40]. Для этих форм с различным размером ячеек моделировался каскад MMC. Мера Λ 3 является точным предиктором средней концентрации в случае γ = 0 для всех форм клеток и немного завышает среднюю концентрацию для γ = 1 мкм с −1 .
Кроме того, мы исследовали различия концентраций между клеточной мембраной и ядром и сравнили их со средней концентрацией в цитозоле. Для сферической клетки средние уровни концентрации в цитозоле, а также на мембране были самыми низкими, что и следовало ожидать, поскольку отношение поверхности к объему является самым низким среди всех форм. Различия в концентрациях между мембраной и ядром были самыми высокими для сферической клетки и клетки с двумя выступами, а средняя концентрация в ядре снизилась почти до нуля для крупных клеток.Для ячейки в форме стержня разница концентраций была наименьшей, так как расстояние вдоль короткой оси мало и концентрация не падает так резко, как для других форм ячейки.
Кроме того, мы установили соответствие эволюции средних уровней концентрации во времени. В случае γ = 0 и произвольной формы ячеек средние уровни концентрации подчиняются системе обыкновенных дифференциальных уравнений (20) (21) (22) где и — средние уровни концентрации в молекулах на площадь клеточной мембраны.Эта система обыкновенных уравнений может быть получена путем интегрирования уравнений (9) — (13) по их соответствующим пространственным областям. См. Приложение S1 для получения подробной информации. Устойчивое состояние для средней концентрации определяется выражением (23) Следовательно, средний уровень концентрации зависит от отношения площади мембраны к цитозольному объему, которое определяется выражением. Таким образом, эффективная скорость глобального фосфорилирования для средней концентрации активных сигнальных молекул в цитозоле определяется величиной. Эти соотношения дают нам соответствие между широко распространенными обыкновенными дифференциальными уравнениями и уравнениями в частных производных для объемной поверхности, используемыми в этой статье.Таким образом, мы имеем сильную зависимость от размера ячеек с уменьшением концентрации для более крупных ячеек.
Эффективный цитозольный транспорт через цитозольные каскады
Далее мы рассматриваем чистый цитозольный (PC) каскад с тремя элементами, в котором все элементы свободно диффундируют через цитозоль. Система реакции-диффузии задается формулой (24) (25) (26) с граничными условиями на мембране (27) (28) и в ядре (29) (30) Обратите внимание, что интерфейс мембрана-цитозоль происходит на первом уровне каскада, а это означает, что только P 1 активируется на мембране со скоростью α 1 P 0 — γP 1 .В частном случае β 1 = β 2 = β 3 = β аналитические аппроксимации цитозольных каскадов в одномерной системе были получены в [41, 42]. В то время как одномерная клеточная геометрия может использоваться для качественного изучения формирования градиента, пространственные эффекты, такие как отношение поверхности клетки к объему, не учитываются. Таким образом, мы получили точные аналитические решения линейной системы в трех измерениях.Устойчивые решения для расширяются следующим образом (31) Алгебраические выражения коэффициентов A n , k и B n , k и их вывод приведены в Приложении S1. По сравнению с каскадом MMC, который обсуждался в предыдущем разделе, третий элемент каскада P 3 более равномерно распределен в ячейке, а градиенты концентрации гораздо более мелкие (см. Рис. 2).
Чтобы количественно определить разницу концентраций в ячейке произвольной формы, мы измеряем дисперсию концентрации в ячейке. Поэтому введем дисперсию как (32) Эта мера близко соответствует дисперсии при анализе изображений [43, 44]. В отличие от анализа изображений, где квадрат отклонения интенсивности флуоресценции от средней интенсивности флуоресценции маркера интегрируется по пикселям, интеграция здесь является непрерывной. Что касается аналога в анализе изображений, нормализованная дисперсия рассчитывается как мера отклонения от среднего [44, 45].Хотя эта мера часто используется в алгоритмах автофокуса при анализе изображений, мы предлагаем нормализованную дисперсию в качестве меры степени локализации сигнальных молекул внутри клетки. Оценка распространения нормализованной дисперсии в цитозольном каскаде дается выражением (33) Здесь C s — постоянная величина, зависящая от формы ячейки, а d — диаметр ячейки. Обратите внимание, что C = C s d — постоянная Пуанкаре из хорошо известного неравенства Пуанкаре [46].Для выпуклой формы ячеек оценка верна для. В случае выпуклой формы клетки небольшой клетки дрожжей (без выступа), следовательно, мы имеем оценку C n ≈ 0,3 ≤ 1 для D cyt = 3 мкм 2 / s , α n = β n = 1 s −1 и диаметр ячейки d = 6 мкм . Для этого набора параметров нормализованная дисперсия уменьшается по крайней мере на 70% на уровне второго цитозольного каскада и на 90% на уровне третьего цитозольного каскада (по сравнению с первым элементом каскада).В общем, для C n <1, нормализованная дисперсия внутриклеточных концентраций уменьшается с увеличением уровня каскада, и различия концентраций в клетке уравновешиваются (см. Фиг.3).
Как и в предыдущем разделе, мы получили оценку средней концентрации. В этом случае мы использовали оценку Λ 1 до, поскольку P 1 является каскадным элементом, который активируется на границе мембрана-цитозоль для каскада ПК.Средняя концентрация связана с величиной, поэтому мы использовали приближение для. Как и в случае с MMC, это приближение является точным для γ = 0 и слегка завышает среднюю концентрацию для γ = 1 мкм s −1 (см. Рис. 3).
Точные выражения для стационарных состояний средней концентрации сигнальных компонентов в случае γ = 0 и для произвольной формы клеток даются выражениями (34) Следовательно, средняя концентрация третьего элемента каскада принимает одинаковые значения в каскаде ММС и ПК.Основное различие обоих пространственных мотивов заключается в том, что различия концентраций, полученные на клеточной мембране и ядре, больше в каскаде MMC, чем в каскаде PC. Как и в предыдущем разделе, мы можем сформулировать систему обыкновенных дифференциальных уравнений для временной эволюции средних концентраций (35) (36) (37) Зависимость абсолютных уровней концентрации от границы раздела мембрана-цитозоль показана на рисунке 2 и рисунке в приложении S1 для набора различных параметров.
Время пространственной сигнализации
Анализ изображений с временным разрешением показал, что сигнальные пути MAPK отвечают измеряемым сигналом в ядре во временных масштабах от секунд до нескольких минут. Ответ пути Hog1 (фосфорилированный MAPK) у почкующихся дрожжей составляет около 80% от его максимальной активности в течение минуты [26]. Другой пример — цикл активации / деактивации Src, в котором колебания и импульсы происходят в режиме секунд [47]. Синхронизация передачи сигнала в линейных сигнальных каскадах для хорошо перемешанных гомогенных систем была проанализирована в [9].Они пришли к выводу, что для слабо активируемых сигнальных каскадов фосфатазы оказывают более выраженное влияние, чем киназы, на скорость и продолжительность передачи сигналов, тогда как амплитуда сигнала контролируется в основном киназами. Тщательный анализ линейных моделей, предполагающих однородное распределение сигнальных молекул для различных видов внешних стимулов, был недавно разработан в [12]. Мы расширили и сравнили эти результаты с пространственной трансдукцией сигнала без упрощения гомогенных концентраций.Сколько времени нужно для установления градиента внутриклеточной концентрации? Как диффузия изменяет время передачи сигнала от клеточной мембраны к ядру? Какие различия концентраций ожидаются, пока не установится устойчивое состояние? Анализ шкалы времени для пространственных моделей сложнее, чем для моделей, основанных на предположениях, смешанных по волеизъявлению, из-за высоких вычислительных затрат. Поэтому мы использовали недавно введенную меру времен накопления [25, 48]. Приближение P n ( r , t ) к его устойчивому состоянию на радиальном расстоянии r от центра ячейки и времени t можно охарактеризовать с помощью функции локальной релаксации. (38) Разницу ρ n ( r , t 1 ) — ρ n ( r , t 2 ) можно интерпретировать как долю установившийся уровень, накопившийся во временном интервале [ t 1 , t 2 ].В бесконечно малом интервале времени [ t , t + dt ] доля накопленных активированных сигнальных молекул в устойчивом состоянии выражается выражением. Время локального накопления определяется как [25] Время накопления может быть получено из стационарного решения, даже если не известна замкнутая форма зависящего от времени решения [25].
Временные характеристики средних концентраций, указанные в системе обыкновенных дифференциальных уравнений для каскада ММС (20) — (22) и каскада ПК (35) — (37), одинаковы и могут быть аналитически выражены как (39) Это выражение также совпадает с временами передачи сигналов, рассчитанными Heinrich et al.[9]. Однако для пространственной модели время локального накопления на мембране и ядре различается. Накопление обычно происходит быстрее на мембране и медленнее в ядре, где степень различия увеличивается с размером клетки (см. Рис. 4). Более того, два пространственных мотива обнаруживают существенные различия. Для каскада MMC время накопления для второго элемента P 2 находится точно на мембране, в то время как для цитозольных видов оно короче (сравните Рис. 4).
Рис. 4. Синхронизация пространственной сигнализации.
Было смоделировано время передачи сигналов для смешанного мембранно-цитозольного (MMC) каскада [слева] и чистого цитозольного (PC) каскада [справа] на мембране и в ядре. ( A ) График зависимости от времени концентраций P 1 , P 2 и P 3 после стимуляции зависимым от времени сигналом. Уровни каскада обозначены цифрами. Обратите внимание, что в случае MMC концентрации для P 1 и P 2 приведены в n M мкм , а концентрация P 3 дана в n. М.Для каскада ПК все концентрации P 1 , P 2 и P 3 приведены в n M. Использованные параметры: R cell = 6 мкм , R nuc = 2 мкм , λ = 1 с −1 , α 1 , α 2 , α 3 = 1.0 с — 1 , β 1 , β 2 , β 3 = 0.5 с -1 , D mem = 0,03 мкм 2 с -1 и D cyt = 3,0 мкм 2 с — 1 . Эта установка была смоделирована для γ = 0 и γ = 1 мкм / s . ( B ) Время накопления для смешанного мембранно-цитозольного каскада. В этом сценарии применялся постоянный сигнал и варьировался размер ячейки.Отношение радиуса клетки к радиусу ядра поддерживалось на уровне R клетки / R nuc = 3. В остальном использовали те же параметры, что и в ( A ).
https://doi.org/10.1371/journal.pcbi.1006075.g004
Время накопления P 3 в ядре, как и ожидалось, намного больше. Для маленьких клеток внутриклеточная концентрация пространственно однородна и приближение сохраняется, в то время как время распространения сигнала к ядру увеличивается с размером клетки.Аналитическое решение времен накопления для P 3 для каскада MMC и частного случая R nuc = 0 может быть получено [49], которое приведено в Приложении S1. Однако для более крупных клеток время распространения сигнала к ядру увеличивается с размером клетки. Для каскада ПК увеличение времени накопления в ядре с увеличением размера клетки менее выражено, чем для смешанно-мембранного цитозольного каскада.
В то время как для расчета времени накопления применялся постоянный стимул, мы также тестировали затухающий сигнал с помощью и численно решили систему, зависящую от времени.Сравнение MMC и PC показано на рис. 4. Интересно, что уровень концентрации на мембране для каскада PC снижается от первого каскада P 1 до второго каскада P 2 и более снова увеличивается от второго каскадного вида P 2 к третьему каскадному виду P 3 , в то время как наблюдается увеличение от предыдущего каскадного вида к следующему каскадному виду в ядре.Это явление вызвано разницей концентраций от клеточной мембраны к ядру, которая для P 1 больше, чем для P 2 в каскаде ПК. Обратите внимание, что параметры были выбраны равными, что означает двукратное увеличение средних уровней концентрации от одного элемента сигнального каскада к другому. Следовательно, пространственная система может вести себя совершенно иначе, чем однородная система. Время накопления на мембране было намного быстрее для γ = 1 мкм / с , чем для γ = 0, и лишь незначительно изменялось с размером ячейки.Однако для более крупных клеток время накопления сигнала в ядре практически не зависело от γ . Следовательно, разница во времени накопления на мембране и ядре увеличилась на γ (также сравните цифру в Приложении S1). В случае каскада ММС время накопления в ядре для клетки с R клетки = 12 мкм почти удвоилось по сравнению с маленькой клеткой с R клетки = 2 мкм , а для В каскаде ПК увеличение времени накопления с размером клеток было менее выраженным.
Для вычисления высших моментов шкалы времени и частного случая клетки без ядра мы ссылаемся на [49]. Анализ временного масштабирования линейного каскада в одном пространственном измерении с четырьмя элементами, включая высшие моменты, был проведен в [50].
Количественная оценка чувствительности пути к пространственно неоднородным сигналам
Далее мы анализируем преобразование разнородных внешних сигналов. Например, в культурах популяций смешанных гаплоидных дрожжевых клеток [40], а также в микрофлюидных устройствах [51] внешний сигнал феромона, который запускает каскад MAPK, не распределяется однородно, а формирует градиенты во внеклеточной среде.Активированный сигнальный каскад пространственно локализован и запускает последующий направленный рост S. cerevisiae [14], а также S. pombe [15]. Более того, свойства белок-белковых взаимодействий и морфологические изменения могут быть тесно связаны [52].
Таким образом, мы исследуем передачу сигнала в ответ на внешний гетерогенный сигнал для клеток той же формы, что и на рис. 3, которые представляли собой сферическую ячейку, ячейку в форме стержня, ячейку с одним выступом и ячейку с двумя выступами.Эти формы клеток встречаются, например, у S. cerevisiae , S. pombe и во время их реакции на стимуляцию феромоном спаривания [53].
Мы протестировали линейный сигнальный каскад с градуированным стимулом вида (40) где и — константы, описывающие базовую мощность сигнала и крутизну сигнала соответственно. Здесь мы выбрали начало координат в центре ячейки и, следовательно,. Таким образом, мы получаем градиент входного сигнала, который линейно увеличивается в направлении x 1 для и линейно уменьшается для.Концентрация при дается выражением.
Мы проверили влияние асимметрии формы клеток в ответ на градиентный стимул (40) и исследовали пространственное распределение последнего сигнального компонента каскада MMC и PC, который равен P 3 . На рис. 5 (A) и 5 (C) профиль концентрации на клеточной мембране, а также вдоль среза клетки в ответ на гомогенный сигнал показан в качестве контроля. Поскольку сферическая ячейка радиально симметрична, градиент на мембране не индуцировался.Для стержневой клетки мы наблюдали неглубокий градиент на поверхности клетки с более высокой концентрацией на полюсах, профиль внутриклеточной концентрации показал две области с низкой концентрацией, которые были разделены ядром. Этот эффект был более выражен для каскада ММС. Для каскада ПК концентрация была почти однородной. Для клеток асимметричной формы с одним и двумя выступами в ответ на однородный входной сигнал был установлен градиент от дистального конца (передний) к сферической части (сзади).Выступ, следовательно, можно сравнить с карманом, в котором устанавливаются более высокие концентрации цитозольных сигнальных молекул. Математически этот эффект можно объяснить геометрической зависимостью собственных функций оператора Лапласа [54], которая может быть использована для характеристики решения уравнений реакции-диффузии для определенной геометрии ячейки. Следовательно, эти асимметричные формы клеток уже могут вызывать градиент сигнальных молекул спереди назад.
Рис 5.Отклик двух каскадных систем, MMC и PC, для различных форм клеток на изменение градиента сигнала.
( A ) Пространственный профиль концентрации на клеточной мембране, а также вдоль среза клетки в ответ на однородный входной сигнал P 0 ≡ 100 n M мкм . Сферическая ячейка имеет размер R ячейка = 2,5 мкм с ядром радиусом R ядер = 1 мкм .Все формы клеток имеют одинаковый объем клеток и содержат сферическое ядро одинакового размера. ( B ) Моделирование для переменного размера ячейки, измеренного как диаметр d x в x-направлении и трех разных наклонах сигнала (зеленый), 0 (оранжевый), 0,03 мкм -1 (красный) были выполнены. Градиент градиента был нанесен. Вот и находятся крайние точки x — направление на клеточную мембрану или ядро. В ( C ) и ( D ) каскады ПК моделировались для той же установки, что и в ( A ), ( B ).Использовались следующие параметры: α 1 = α 2 = α 3 = 1 с −1 , β 1 = β 2 = β 3 = 1 с -1 , γ = 0,5 мкм с -1 , D mem = 0,03 мкм 2 с -1 и D cyt = 3.0 мкм 2 с -1 .
https://doi.org/10.1371/journal.pcbi.1006075.g005
На рис. 5 (B) и 5 (D) отклики на сигнал с, увеличивающимся в направлении x 1 . , и сигнал с, который уменьшается в направлении x 1 , были смоделированы и противопоставлены ответу на пространственно однородный сигнал с помощью. Для измерения отклика мы естественным образом определяем градиент n -го элемента каскада как разность концентраций в двух точках на евклидовом расстоянии этих двух точек.В случае концентраций киназы градиент рассчитывали из. Здесь и находятся крайние точки в x 1 -направлении на клеточной мембране или ядре. Оба мотива, каскад MMC и PC, по-разному ведут себя при передаче градиентов сигнала. Градиент уровня третьего каскада P 3 вдоль клеточной мембраны и ядра уменьшался для каскада MMC с размером клеток для всех форм. Для ПК градиент увеличивался с размером ячейки до максимального значения, а затем уменьшался с увеличением размера ячейки, что предполагает оптимальный размер ячейки для обнаружения и передачи градиента.Этот эффект был ожидаемым, поскольку для маленьких клеток концентрация в цитозоле была почти однородной, а различия в концентрациях уравновешивались диффузией. Однако с увеличением размера клетки средний уровень концентрации в клетке и ядре снижался. Как следствие, также уменьшился абсолютный градиент.
Ячейка в форме стержня показала более сильный ответ, чем ячейка сферической формы, поскольку концентрации были выше на полюсах и ячейка была выровнена по градиенту.Кроме того, компартментализация, индуцированная ядром в клетке в форме тонкого стержня, оказала выраженное влияние на градиент P 3 , поскольку диффузия в цитозоле спереди назад была затруднена. Для ячеек с одним и двумя выступами градиент P 3 был сильно смещен с увеличением направления выступов. Обратите внимание, что оба мотива ведут себя по-разному при передаче градиента ядру. В то время как для каскада MMC зависимость формы была более выраженной, а градиент внутри клетки был почти отделен от градиента на мембране для асимметричных форм клеток, каскад ПК передавал градиент более надежно внутрь клетки и в ядро.
Итак, мы наблюдали сильное влияние размера клеток на локализацию и установление градиентов с помощью элементов сигнального каскада. Для ячейки с выступом концентрация P 3 в выступе была выше, чем в противоположном дистальном конце, который является сферической частью ячейки. Этот эффект возник из-за более высокого отношения локальной поверхности к объему в области выступа. Следовательно, большая часть цитозольных сигнальных молекул, которые свободно диффундируют в цитозоле, фосфорилируется в части выступа, приводя к градиенту от кончика выступа к противоположному дистальному концу клетки.Влияние клеточной асимметрии также исследовалось в [23] для градиентов малой Rho-GTPase Cdc42 во время клеточной поляризации. Однако эта система реагирует противоположным образом, поскольку поток молекул при установлении сайта полярности направлен из цитозоля на мембрану и, следовательно, устанавливается градиент от дистального конца к выступу.
Эти эффекты возникают из-за разной архитектуры обеих систем. В сигнальных каскадах ПК и ММС мы имеем передачу сигнала от мембраны к ядру и, следовательно, диффузионный поток активированных сигнальных молекул из мембраны в цитозоль, тогда как в системе поляризации поток сигнальных молекул во время установления сайт полярности направлен из цитозоля на мембрану, что является противоположным направлением.Следовательно, обе системы по-разному реагируют на клеточную асимметрию относительно образования градиента. Это взаимодействие обеих систем особенно интересно, поскольку у многих организмов поляризационная система взаимодействует с каскадом MAPK [55, 56] и, следовательно, может точно контролировать форму и размер клеток.
Для сферической формы ячеек мы, кроме того, исследовали более сложные градиенты внешнего сигнала, то есть неоднородности с множеством максимумов и минимумов (см. Приложение S1). Как и в [18, 57], неоднородный сигнал на сфере можно разложить с помощью сферических гармоник (41) (42) В этом разложении амплитуды более высокого порядка, где порядок обозначен как -1, обычно более сильно затухают, чем градиенты или пространственные неоднородности более низкого порядка.Таким образом, результаты, показанные здесь, могут быть расширены до сложных пространственных сигналов на поверхности клетки. Мы предоставляем полные аналитические решения для MMC и PC для сферы без ядра (см. Приложение S1).
Системы с обратной связью
В этом разделе мы анализируем влияние размера клетки на передачу сигнала для осциллирующего каскада, состоящего из двух мембраносвязанных и одного цитозольного элемента (MMC), и каскада из трех цитозольных элементов (PC), то есть для M = 2 и M = 0 соответственно.Далее исследуется случай отрицательной обратной связи и постоянного однородного сигнала.
Отрицательные обратные связи являются частым элементом регуляции сигнальных каскадов и могут быть индуцированы дефосфорилированием вышележащих компонентов с помощью MAPK или фосфатаз [39, 58–61]. Примеры представлены фосфатазами Tyr, которые могут вызывать отрицательную обратную связь [47], и фосфатазами двойной специфичности (DUSP) [59]. Некоторые отрицательные обратные связи, например, индуцированные в цикле Src-Tyr, приводят к колебаниям на временной шкале секунд [47], в то время как другие действуют на гораздо более длительных временных масштабах.Например, во время дрожжевой феромонной реакции MAPK Fus3 подвергается устойчивым колебаниям в течение 2-3 часов, которые контролируют периодическое образование спаривающихся выступов. В этом процессе Sst2 действует как негативный регулятор передачи сигналов G-Protein на мембране, тогда как дезактивация в цитозоле опосредуется MAPK фосфатазой Msg5 [39]. Классическим и наиболее простым примером осциллятора с отрицательной обратной связью и нелинейными членами реакции является колебательная система Гудвина [62, 63].
Мы адаптируем упомянутую модифицированную систему и формулируем задачу, используя уравнения в частных производных, добавляя диффузионный член и формулируя граничные условия в соответствии с моделями, упомянутыми ранее. Скорости фосфорилирования и дефосфорилирования для обеих моделей читаются как (43) (44) (45) согласно уравнениям (1) — (5) соответственно. Скорость активации содержит отрицательную обратную связь, поскольку высокая концентрация P 3 приводит к более низкой активации P 1 .Предположим постоянный внешний сигнал.
Для первой модели (MMC) дезактивация со скоростью происходит в цитозоле, тогда как активация происходит на мембране и поэтому моделируется как граничное условие с v i = 0 в соответствии с уравнениями (2 ) и (3), поскольку P 3 является исключительно цитозольным видом. Мы предполагаем условия нулевого потока для P 3 на ядре, что означает, что мы устанавливаем скорость реакции ядерного импорта ϵ = 0 (сравните уравнение (8)).
Для второй модели (PC) все виды являются исключительно цитозольными, поэтому скорость активации для P 1 является граничным условием, описывающим активацию P 1 на мембране. Мы предполагаем условие нулевого потока для P 3 на ядре ( ϵ = 0) и для P 1 и P 2 как на ядре, так и на мембране, что означает всю границу.
Обе модели имеют нелинейную кинетику, а также отрицательную обратную связь, приводящую к колебаниям.Кроме того, в обеих моделях скорость активации для P 1 зависит от параметра p > 0. Это показано, например, в [64], что для p > 8 система ODE, состоящая из трех компонентов, дестабилизируется, а для более длинных каскадов, т.е. для большего N , система становится нестабильной для еще более низких значений p > 1.
Поскольку аналитическое решение для обеих моделей неизвестно, для решения систем необходимо использовать численные методы.По причинам простоты и из-за больших вычислительных затрат мы решили системы в двух измерениях, используя диск для моделирования ячейки. Мы использовали схему с фиксированной точкой для решения нелинейных уравнений.
Выбраны параметры β 1 = β 2 = β 3 = 0,125 с −1 , D cyt = 1 мкм 2 с -1 , D mem = 0.01 мкм 2 s −1 , R nuc = 1 мкм и R ячейка = 2 мкм . Начальные условия: P 1 = P 2 = 10 n M мкм и P 3 = 10 n M для каскада MMC и P 1 = P 2 = P 3 = 10 n M для каскада ПК.Для K m = 100 n M и силы обратной связи p = 10, обе модели колебались, как и ожидалось, рис. 6A.
Рис. 6. Колебания в зависимости от размера в системе с отрицательной обратной связью.
( A ) Средняя концентрация P 1 , P 2 и соответственно P 3 с течением времени. После начального пика обе системы колеблются. Обратите внимание, что в случае MMC, P 1 , P 2 уровни концентрации приведены в n M мкм , а P 3 концентрация дана в n M.Для каскада ПК все концентрации P 1 , P 2 и P 3 приведены в n M. ( B ) Частотный анализ средней концентрации обеих моделей для последний вид, P 3 . ( C ) Частота и амплитуда средней концентрации P 3 для двух моделей в зависимости от размера ячейки.
https://doi.org/10.1371 / journal.pcbi.1006075.g006
Следовательно, в случае относительно небольшого размера ячейки R ячейки = 2 мкм , обе пространственные модели ведут себя аналогично исходной модели, которая была сформулирована как система обыкновенных дифференциальных уравнений. Анализ частот колебаний и средней концентрации можно увидеть на рис. 6В. Основываясь на предыдущих экспериментах и графиках, частотный анализ был проведен после t = 200 s , когда частоту и соответствующие амплитуды средних концентраций для обеих моделей можно считать постоянными.Обе модели показывают очень похожее поведение, тогда как частота и средняя концентрация выше для чистой цитозольной модели, что можно объяснить тем фактом, что реакции происходят не только на мембране, но и повсюду в цитозоле.
На следующем этапе мы изменили размер ячейки 1,5 мкм ≤ R ячейка ≤ 4,0 мкм и снова провели анализ частот и соответствующих амплитуд для обеих моделей. Результаты анализа третьего компонента обеих моделей представлены на рис. 6С.Как указывалось ранее, частота для обеих моделей очень похожа, но амплитуда сигнала выше для цитозольной модели.
Колебания в первой, смешанной каскадной модели возникают только для размера ячейки до R ячейки ≤ 2,5 мкм , а во второй, чистой цитозольной модели для размера ячейки до R ячейки ≤ 3,0 мкм . Начальные колебания быстро затухают, и обе модели сходятся к установившемуся состоянию, если размер ячейки выбран больше.
Discussion
Стимулируемые прогрессом в области визуализации клеток и растущей потребностью в понимании внутриклеточной динамики, мы исследовали и обсудили общий подход к моделированию передачи клеточного сигнала во времени и пространстве. Сигнальные каскады ковалентных модификаций белков, такие как каскады митоген-активируемой протеинкиназы (MAPK) и небольшие каскады GTPase, встречаются во множестве вариаций [1, 13, 65]. Первый сигнальный компонент может быть активирован на клеточной мембране с помощью связанного с мембраной фермента, такого как киназа или фактор обмена гуаниновых нуклеотидов в передаче сигналов GTPase, в то время как дезактивация может происходить на мембране или в цитозоле, например, опосредованной фосфатазой. или белок, активирующий ГТФазу [66].Следовательно, активация и деактивация могут быть пространственно разделены, что создает ряд различных пространственных расположений и комбинаций при передаче сигнала.
Мы исследовали сигнальные каскады с различным пространственным расположением сигнальных компонентов. Мы показали, что моделирование интерфейса мембрана-цитозоль имеет решающее значение, а также соотношение площади мембраны и цитозольного объема, которые являются пространственными свойствами. Результаты свидетельствуют о сильной зависимости передачи сигнала внутри клеток от размера и формы клеток, которые, вероятно, вносят вклад в изменение отдельных клеток в ответ на внеклеточные стимулы.Мы предлагаем, чтобы клетки измеряли отношение клеточной мембраны к объему клетки, чтобы координировать рост и дифференцировку. Для асимметричных форм клеток также важны локальные изменения в соотношении объема клетки к клеточной мембране для внутриклеточной передачи сигналов. Широко используемые зависящие от времени модели обыкновенных дифференциальных уравнений могут быть естественным образом распространены на пространство с помощью дифференциальных уравнений объемной поверхности. Применяя это расширение к классу моделей линейной передачи сигнала, мы сравнили предположение о хорошо перемешанной клетке с двумя различными мотивами передачи пространственного сигнала.Мы вывели и обсудили критерии, которые можно использовать для проверки хорошо смешанного предположения, и показали, что кинетика, которая связывает мембраносвязанные виды с цитозольными видами, естественным образом вызывает зависимость от размера. Таким образом, результаты имеют важное значение для кинетических моделей передачи сигналов.
Наши результаты имеют важное биологическое значение. Поскольку сигналы, передаваемые линейными сигнальными каскадами от клеточной мембраны к ядру, экспоненциально уменьшаются в масштабе нескольких микрон, наши теоретические результаты предполагают сильную зависимость размера клетки в ответ на внеклеточные стимулы.Кроме того, отношение общего объема клетки к площади клеточной мембраны важно для средних уровней концентрации. Проекции спаривания, возникающие у дрожжей, действуют как карманы для сигнальных молекул, которые могут поддерживать биохимические обратные связи. Адаптации в виде ламеллиподий в кератоцитах или инвагинаций, таких как Т-канальцы в миоцитах, могут локально увеличивать накопление сигнальных молекул. Эти клеточные структуры способны напрямую обеспечивать обратную связь при передаче сигналов.
Мы предлагаем нормированную дисперсию в качестве меры для количественной оценки различий в концентрациях и локализации сигнальных молекул, которые могут быть получены из данных микроскопии с пространственным разрешением в дополнение к средним уровням интенсивности маркера флуоресценции.Например, было бы полезно измерить среднюю концентрацию и нормированную дисперсию вместе с размером и морфологией клеток. В интересных исследованиях ответа в популяциях клеток часто отсутствует поведение ответа, связанное с размером и морфологией клеток. Примеры варьируются от поведения переключателя в популяциях ооцитов [67] до феромонного ответа в дрожжевых клетках [68, 69]. Следовательно, данные об отдельных клетках, в которых размер клетки назначается этим измерениям, необходимы для точного количественного исследования пути, чтобы отделить биохимические свойства белок-белковых взаимодействий и морфологические свойства, такие как размер и форма целых клеток.Нацеливание на сигнальные белки с помощью модификаций липидирования, таких как пальмитоилирование, пренилирование или миристоилирование [2, 3, 5], может изменить секвестрацию сигнального каскада с чистого цитозольного (PC) каскада на каскад со смешанными мембранами (MMC). В случае ММС со смешанной мембраной зависимость от геометрии и размера более выражена, поскольку первые сигнальные элементы привязаны к мембране. Напротив, для исследуемого каскада ПК локализация и сильные внутриклеточные градиенты уменьшаются, но в зависимости от кинетических параметров геометрическая информация также может лучше передаваться по всей клетке.
В нелинейных сигнальных системах различия, которые мы наблюдали в моделях линейных сигнальных каскадов, вероятно, будут усиливаться. Нелинейная кинетика может усиливать образование градиента, что приводит к еще более сильным различиям внутриклеточных концентраций [70]. Это также справедливо для уровней абсолютной концентрации, которые могут переключаться в зависимости от кинетики [67, 71]. Более того, кинетика более высокого порядка может усиливать разницу во времени накопления в разных клеточных местоположениях [72], что может приводить к пространственным колебаниям и фосфопротеиновым волнам.
Анализ модели сигнального каскада может быть расширен на более сложные пространственные неоднородности, например, с помощью ряда Лапласа, как предложено в [18, 57]. С помощью этого подхода могут быть представлены локализованные сигналы, возникающие из мембранных структур, таких как липидные рафты, септины или совместная локализация из-за белок-белковых взаимодействий. Поскольку они часто являются предшественниками формы клеток и структур органелл, взаимодействие с формой и морфологией клеток должно быть рассмотрено в будущих исследованиях.Зависимость внутренней геометрии сигнальных систем недавно была показана для эллипсоидальных форм клеток в системе MinE-MinD [24, 73, 74], но также и в дрожжевой системе [23, 75–77]. Ожидается, что последние разработки математических методов, таких как метод конечных элементов для уравнений объемной поверхности [19, 20], а также методы анализа устойчивости этих систем [23, 78–82], дадут дальнейшее понимание поведения передачи клеточного сигнала.


 :
: